范文一:有机物的结构简式
有机物的名称、分子式和结构简式
编名 称 分子式 结 构 ,简, 式 号
烷 烃 1 甲烷 CH4
2 乙烷 CH26
CH—CH、CHCH、 3333
CH—CH—CH、CHCHCH、 3233233 丙烷 CH38
、 4 正丁烷 CHCH—CH—CH—CH、CHCHCHCH、 410 32233223
2—甲基丙烷 5 CH410 ,异丁烷, 、CH,CH,、 33
CH—CH—CH—CH—CH、CHCHCHCHCH、 32223322236 ,正,戊烷 CH512 CH,CH,CH、 3233
2—甲基丁烷
7 CH,异戊烷, 512
2 ,2—二甲基丙
烷 8 CH512 ,新戊烷,
、C,CH,34
CH—CH—CH—CH—CH—CH、 3222239 正己烷 CH614 CHCHCHCHCHCH、CH,CH,CH、 3222233243
2—甲基戊烷 10 CH614 ,异己烷, 11 3—甲基戊烷 CH614
2 ,3—二甲基丁12 CH614 烷
2 ,2—二甲基丁13 CH614 烷
CH—CH—CH—CH—CH—CH—CH、 322222314 ,正,庚烷 CH716 CHCHCHCHCHCHCH、CH,CH,CH32222233253
2—甲基己烷 15 CH716 ,异庚烷, 16 3—甲基己烷 CH716
2 ,2—二甲基戊17 CH716 烷
3 ,3—二甲基戊18 CH716 烷
2 ,3—二甲基戊19 CH716 烷
2 ,4—二甲基戊20 CH716 烷
2 , 2 ,3—三甲21 CH716 基丁烷
3—乙基戊烷 22 CH716
2,2,4,4—四甲23 CH920 基戊烷
2,3—二甲基—24 CH920 3—乙基戊烷
3 ,3,4—三甲基25 CH920 己烷
2,2,4—三甲基26 CH818 戊烷
2,3,3—三甲基27 CH818 戊烷
2,2,3—三甲基28 CH818 戊烷
2,3,4—三甲基29 CH818 戊烷
环 烷 烃 30 环丙烷 CH 36、 31 环戊烷 CH 510
、 32 环己烷 CH 612
、、 33 甲基环己烷 CH 714
、 34 乙基环己烷 CH 816
顺对二甲基环35 CH 816己烷
反对二甲基环36 CH 816己烷
烯 烃
37 乙烯 CH24 CH,CH、 22
33 丙烯 CHCH—CH,CH、CHCH,CH 36 323234 1—丁烯 CHCH,CH—CH—CH、 48 22335 2—丁烯 CHCH—CH,CH—CH、CHCH,CHCH 48 333336 甲基丙烯 CH48
CH,CH—CH—CH—CH、 222337 1—戊烯 CH510 CH,CHCHCHCH、CH,CH,CH,CH 22232223
CH—CH,CH—CH—CH、 32338 2—戊烯 CH510 CHCH,CHCHCH 323
2—甲基—1—39 CH510 丁烯
3—甲基—1—40 CH510 丁烯
2—甲基—2—41 CH510 丁烯 42 1 ,3—丁二烯 CHCH,CH—CH,CH、CH,CHCH,CH 46 2222
2—甲基—1 ,3
—丁二烯 43 CH58 ,异戊二烯,
2,2,5,5—四甲44 CH1020 基—3—己烯 、
,CH,CCH,CHC,CH, 3333
2,4,4—三甲基45 CH816 —1—戊烯
2,4,4—三甲基46 CH816 —2—戊烯
3—甲基—1,347 CH814 —己二烯
2—甲基—
48 3,2,2—乙基,—CH916
1,3—丁二烯
3,4—二甲基—
49 2—乙基—1—CH918
戊烯
3—乙基—1 ,350 CH712 —戊二烯
51 4—甲基环己烯 CH712
炔 烃
52 乙炔 CHHC?CH、H—C?C—H 22
丙炔 HC?C—CH、CH?CCH 53 CH3334
54 1—丁炔 CHHC?C—CH—CH、CH?CCHCH、 46 232355 2—丁炔 CHCH—C?C—CH、CHC?CCH 46 333356 1—戊炔 CHHC?C—CH—CH—CH、CH?CCHCHCH、 58 22322357 2—戊炔 CHCH—C?C—CH—CH、CHC?CCHCH 58 323323
3—甲基—1—58 CH58 丁炔
3—甲基己—359 CH710 —烯炔
3—乙基戊—360 CH710 —烯炔
芳 香 烃
61 苯 CH66 、、 62 甲苯 CH78
、、CH—CH653 63 乙苯 CH810
、、CH—CH 652564 邻二甲苯 CH810
间二甲苯 65 CH810
66 对二甲苯 CH810 67 间甲乙苯 CH912
戊苯 68 CH1116 CHCH、 65511
69 2—苯基戊烷 CH1116
2—甲基—1—70 CH1116 苯基丁烷
3—甲基—1—71 CH1116 苯基丁烷
2—甲基—3—72 CH1116 苯基丁烷
2,2—二甲基—73 CH1116 1—苯基丙烷 、CHCHC,CH, 65233
74 3—苯基戊烷 CH1116 、CHCH,CHCH,65232 75 苯乙烯 CH88
、、CHCH,CH652 76 苯乙炔 CH86 、CHC,CH 6577 联二苯 CH1210 、CH—CH、,CH,6565652
二苯甲烷 78 CH1212 、CH,CH,2652 79 萘 CH108
80 ,—甲萘 CH1110
81 ,—甲萘 CH1110
82 1,6—二甲萘 CH1212
83 1,5—二甲萘 CH1212
84 ,—乙萘 CH1212
85 ,—乙萘 CH1212
86 蒽 CH1410 87 菲 CH1410 88 并四苯 CH1812 89 并五苯 CH2214
90 CH1610
91 CH2212
卤 代 烃
92 一氯甲烷 CHCl CHCl 33
93 二氯甲烷 CHCl CHCl2222 94 三氯甲烷,氯仿, CHCl CHCl 3395 四氯化碳 CClCCl4 4 96 三碘甲烷,碘仿, CHI CHI 3397 四氟化碳 CFCF 4 498 四溴化碳 CBrCBr 4 499 四碘化碳 CICI 4 4100 氯乙烷 CHCl CHCl、CHCHCl 252532101 溴乙烷 CHBr CHBr、CHCHBr 252532102 氯苯 CHCl 65、CHCl 65103 溴苯 CHBr 65、、CHBr 65104 四氟乙烯 CF CF,CF2422
1,1,2,2—四溴105 CHBr CHBr—CHBr22422 乙烷
106 1,2—二溴乙烯 CHBr BrCH,CHBr 222
107 氯乙烯 CHCl CH,CHCl 232
3,4—二溴—1108 CHBr CH,CH—CHBr—CHBr 46222—丁烯
1,4—二溴—2109 CHBr CHBr—CH,CH—CHBr 46222—丁烯
110 邻氯甲苯 CHCl 77
111 间氯甲苯 CHCl 77
112 对氯甲苯 CHCl 77
2,4,6—三溴甲113 CHBr753 苯
114 苄氯,苯甲氯, CHCl 77
115 4—溴辛烷 CHBr817 、CH,CH,CHBr,CH,CH323223
醇
116 甲醇 CHO CH—OH、CHOH 433117 乙醇 CHO CH—OH、CHOH、CHCHOH 26252532118 1—丙醇 CHO CH—OH、CHOH、CHCHCHOH 383737322
2—丙醇,异丙119 CHO 38醇,
1— 丁醇 H—OH、CHOH、CH,CH,OH C120 CHO 4949323410,正丁醇,
2—丁醇 121 CHO 410,异丁醇,
2—甲基—1—122 CHO 410丙醇
2—甲基—2—123 CHO 410丙醇
、
2,2—二甲基—124 CHO 5121—丙醇
2—甲基—2—125 CHO 512丁醇
、、 126 乙二醇 CHO262 、HOHCCHOH、,CHOH,2222 127 丙三醇 CHO383
、CH,OH,353
2—丁炔—1,4128 CHO462 二醇 129 氨基乙醇 CHNO27
2,2—二甲基—130 CHO 6141—丁醇
3—甲基—1—131 CHO 512丁醇
2—戊醇 132 CHO 512、 133 3—戊醇 CHO 512
134 1,2—丁二醇 CHO41142 135 2—氯乙醇 CHOCl 25 136 苯甲醇,苄醇, CHO 78
137 环丙醇 CHO36 138 对甲基环己醇 CHO 714
139 邻甲基环己醇 CHO 714
醚
140 甲醚 CHO CH—O—CH、CHOCH 263333141 甲乙醚 CHO CH—O—CH、CHOCH、CHOCHCH 38325325323
H—O—CH、CHOCH、 C25252525142 乙醚 CHO 410CHCHOCHCH、,CH,O3223252 143 甲正丙醚 CHO CH—O—CH、CHOCH、CHOCHCHCH 4103373373223
144 甲异丙醚 CHO 410
CHOCH,CH,、 332145 甲苯醚 CHO 718 146 异丙醚 CHO 614、,CH,CHOCH,CH, 3232
环 氧 烷 147 环氧乙烷 CHO 24 148 二氧杂环己烷 CHO 48
149 甲基环氧乙烷 CHO 36
酚
150 苯酚 CHO 66
、
1,2,3—苯三酚 151 CHO663 ,邻苯三酚,
1,3,5—苯三酚 152 CHO663 ,间苯三酚,
2,4,6—三溴苯153 CHObr633 酚
、 154 邻甲苯酚 CHO78
155 间甲酚 CHO78
156 对甲酚 CHO78
2,4,6—三硝基157 CHNO6337 苯酚
醛 和 酮 158 甲醛 CHO 2HCHO、
乙醛 159 CHO 24CHCHO、 3
160 丙醛 CHO CHCHCHO、CHCHO 363225161 丁醛 CHO CHCHCHCHO、CHCHO 4832237
162 2—甲基丙醛 CHO 48、,CH,CHCHO 32163 3—丁羟醛 CHO482 164 乙二醛 CHO222 、、,CHO,2 165 丙酮 CHO 36、、
,CH,CO、CHCOCH3233 166 丁酮 CHO 48、CHCOCHCH323 167 丙二烯酮 CO32
O,C,C,C,O、
邻乙酰基苯乙168 醛
羧 酸
169 甲酸 CHO22 HCOOH、、 170 乙酸 CHO242 CHCOOH、 3
171 丙酸 CHO362 CHCHCOOH、CHCOOH、 3225172 丁酸 CHOCHCHCHCOOH、CHCOOH 482 32237173 甲基丙酸 CHO482 、,CH,CHCOOH 32174 硬脂酸 CHO18362 CHCOOH、 1735
175 软脂酸 CHO16322 CHCOOH、 1531
油酸 176 CHOCHCOOH 18342 1733
、、 177 苯甲酸 CHO762
CHCOOH、 65
178 苯正丙酸 CHO9102
、CHCHCHCOOH 6522179 乙二酸 CHO224 、、
,COOH,、HOOC—COOH 2
180 丙二酸 CHO344
、HOOC—CH—COOH、CH,COOH,222 181 丁二酸 CHO464 、HOOC,CH,COOH、,CHCOOH,2222 182 顺丁烯二酸 CHO444
183 反丁烯二酸 CHO444 184 邻苯二甲酸 CHO864
185 间苯二甲酸 CHO864
186 对苯二甲酸 CHO864 187 甲,酸,酐 CHO,HCO,O 223 2188 乙酐 CHO463 、,CHCO,O 32
乳酸 189 CHO363 ,,—羟基丙酸, 、
,—羟基丙酸 190 CHO363
2,2—二甲基丙191 CHO4102 酸
、,CH,CCOOH 33
3—甲基戊—4192 CHO6122 —烯酸 193 邻羟基苯甲酸 CHO763 194 对羟基苯甲酸 CHO763
、
间羟基苯甲酸 195 CHO763
对羟基苯—2—196 CHO983 丙烯酸
间羟基羧基苯197 CHO884 甲醇
酯
198 甲酸甲酯 CHOHCOOCH、242 3 199 甲酸乙酯 CHOHCOOCH、HCOOCHCH362 2523
乙酸甲酯 200 CHO362 、CHCOOCH33 201 乙酸乙酯 CHO、 482
CHCOOCH、CHCOOCHCH325323 202 甲酸正丙酯 CHOHCOOCH、HCOOCHCHCH482 37223 203 甲酸异丙酯 CHO482
、、HCOOCH,CH,32
甲酸新戊酯、
204 甲酸,2,2—二甲CHO6122
基,丙酯 、HCOOCHC,CH, 233
甲酸—2—甲基205 CHO6122 丁酯
206 甲酸异戊酯 CHO6122 、HCOO,CH,CH,CH,2232 207 对乙酸甲苯酯 CHO9102
丙酸甲酯 CHCHCOOCH、CHCOOCH208 CHO323253 482
对羟基苯甲酸209 CHO883 甲酯
2,2—二甲基丙
210 酸甲酯、 CHO6122
新戊酸甲酯 、,CH,COOCH333 211 硬脂酸甘油酯 CHO571106
、,CHCOO,CH173535 212 软脂酸甘油酯 CHO511706
、,CHCOO,CH 153135213 油脂酸甘油酯 CHO571046
、,CHCOO,CH 173335214 苯甲酸甲酯 CHO882 、CHCOOCH653 215 硝酸乙酯 CHNO CHONO、CHCHONO 253252322
3—羟基丙酸正216 CHO6123 丙酯 、HO,CH,COO,CH,CH22223
2—羟基丙酸正217 CHO6123 丙酯 218 丙二酸二乙酯 CHO7124
、CHOOC—CH—COOCH25225
2—丁酮酸异丁219 CHO8143 酯 220 乙酸对甲酚酯 CHO9102 221 甲酸氯甲,醇,酯 CHOCl 232 222 异戊酸异戊酯 CHO10202 、
,CH,CHCOO,CH,CH,CH, 32232
乙二酸乙二,醇,223 CHO444 酯
三硝酸甘油酯 224 CHNO3539 ,硝化甘油,
硝 基 化 合 物
225 硝基苯 CHNO652 、、CH—NO 652226 硝基甲烷 CHNOCH—NO、CHNO 32 3232227 硝基乙烷 CHNOCH—NO、CHNO、CHCHNO 252 252252322
2,4,6—三硝基228 CHNO7536 甲苯,TNT,
229 ,—硝基萘 CHNO1072
230 ,—硝基萘 CHNO1072
1,8—二硝基萘 231 CHNO10624
232 1,5—二硝基萘 CHNO10624
糖 类 233 葡萄糖 CHO6126
、CHOH,CHOH,CHO 24234 果糖 CHOCHOH,CHOH,COCHOH 6126 232235 蔗糖 CHOCHO122211 122211 236 麦芽糖 CHOCHO122211 122211 237 淀粉 ,CHO,,CHO, 6115n 122211n238 纤维素 ,CHO,6115n
、[CHO,OH,] 6723n
氨 基 酸
甘氨酸 239 CHNO252 ,氨基乙酸,
丙氨酸 240 CHNO372 ,—氨基丙酸
苯丙氨酸
241 ,—氨基—,—CHNO8112
苯基丙酸
谷氨酸 242 CHNO594 ,—氨基戊二酸
高 分 子 化 合 物 243 聚乙烯 ,CH,24n 244 聚丙烯 ,CH,36n
245 聚氯乙烯 ,CHCl,23n
246 聚苯乙烯 ,CH,88n
、
有机玻璃,聚甲247 ,CHO,582n 基丙烯酸甲酯,
、
聚丙烯腈 248 ,CHCN,23n ,人造羊毛,
聚四氟乙烯 249 ,CF,24n ,塑料王, 250 酚醛塑料,电木, ,CHO,76n
251 脲醛塑料,电玉, ,CHNO,42n
252 环氧树脂 ,CHO,19203n
聚对苯二甲酸
253 乙二醇酯 ,CHO,10103n ,涤纶、的确良,
聚己内酰胺 254 ,CHNO,611n ,绵纶,
聚乙烯醇缩甲
255 醛 ,CHO,582n ,维尼纶,
256 丁苯橡胶 ,CH,1214n
257 顺丁橡胶 ,CH,46n 258 氯丁橡胶 ,CHCl,45n 259 丁腈橡胶 ,CHCN,79n
260 聚硫橡胶 ,CHS,244n 261 硅橡胶 ,CHSiO,26n
262 丁基橡胶
异戊橡胶 263 ,CH,58n ,合成天然橡胶, 264 聚乳酸 ,CHO,332n 265 聚丙酸甲酯 ,CHO,462n
266 聚丙酸正丁酯 ,CHO,7122n
267 聚乙丙丁酯 ,CH,918n
268 人造象牙 ,CHO,2n 289 聚环氧乙烷 ,CHO,24n 290 聚乙炔 ,CH,22n 291 ,CH,916n
292 戊苯橡胶 ,CH,1316n
293 ,CH,1010n
294 ,CH,1010n
295 Nomex纤维 ,CHNO,141022n
296 ,CHO,15166n
其 它 297 二恶英 ,CHOCl,12424n
298 维生素C ,CHO,686n
299 立方烷 ,CH,88n
2,3,4—三羟基
苯甲酸—2,3—300 ,CHO,14109n 二羟基—5—羧
基苯,酚,酯 301 苯磺酸 CHSO663
302 对氨基苯磺酸 CHNSO1093
303 吗啡 CHNO17173
304 葡萄糖二酸 CHO6108
三硝酸纤维素305 ,CHNO,6739n 酯
丙二酰氯 306 CHOCl3222
307 丙二酰胺 CHNO3622
3,7—二甲基—308 CHO1016 2,6—辛二烯醛
三聚甲醛 309 CHO363
310 氨基树脂 CHN666
范文二:苯 的结构简式是
苯 的结构简式是 ----1----或 ----2----,苯分子中, 6个碳原子连接成 ---3----结构, 碳原子间的化学键是一种 -------4--------的特殊的共价键, 6个碳原子和 6个氢原子完全等价, 人们称苯的这种特殊结构为 ----5------。把苯倒入盛满水的试管中震荡,静止后发现 --------6---------,说明苯的密度比水 ----7------, ----8-----溶于水。若在上述试管中加入少量碘水震荡, 静止,又发现 --9----,说明苯是很好的 ---10---剂。
1. 如图片中下方
2. 一个 ,中间一个圆
3. 平面
4. 既不同于碳碳单键也不同于
5.
6. 溶液分层,苯在上层
7. 小
8. 不
9. 溶液分层,上层显紫色
10. 非极性溶
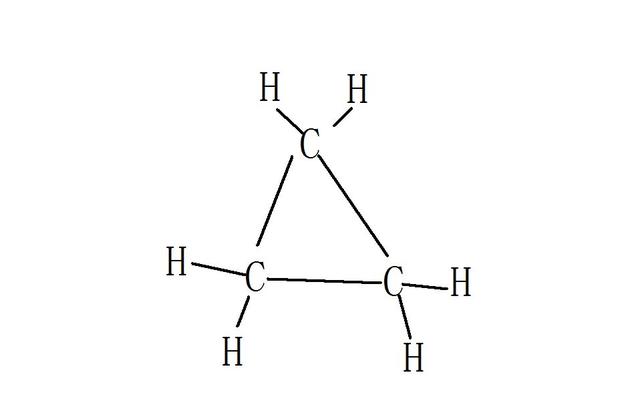
环己烷 的结构简式
范文三:苯的结构简式是
的结构简式?是----1----或----2----,苯分子中,6个碳原子?连接成---3----结构,碳原子间的?化学键是一?种-------4--------的特殊的共?价键,6个碳原子?和6个氢原?子完全等价?,人们称苯的?这种特殊结?构为----5------。把苯倒入盛?满水的试管?中震荡,静止后发现?--------6---------,说明苯的密?度比水----7------,----8-----溶于水。若在上述试?管中加入少?量碘水震荡?,静止,又发现--9----,说明苯是很?好的---10---剂。
1.如图片中下?方
2.一个正六边形,中间一个圆?
3.平面正六边形
4.既不同于碳?碳单键也不?同于碳碳双键
5.大π键
6.溶液分层,苯在上层
7.小
8.不
9.溶液分层,上层显紫色?
10.非极性溶
环己烷 的结构简式?
范文四:结构简式
乙 醇
[思考]酒精中含有少量的水,如何检验?如何除去?
3、化学性质: (1) 置换反应: 思考:为什么比水反应慢? (2)氧化反应:
思考:铜丝的作用是什么?
说明:有机化学中“失氢”称为氧化反应,“得氢”称为还原反应。
[讨论]:
1、 乙醇有哪些用途?
2、 请写出甲醇、乙二醇的结构简式,并指出其用途。 3、 写出乙醛的结构式和分子式
4、 写出乙醛加氢还原变成乙醇的化学方程式。
[例题] 为了确定乙醇分子的结构简式是CH3—O—CH3还是CH3CH2OH,实验室利用如图所示
无水乙醇 的实验装置,测定乙醇与钠反应(△H<0)生成氢气的体积,
并据此计算乙醇分子中能与金属钠反应的氢原子的数目。
导管B
导管 试回答下列问题:
A
①指出实验装置中的错误 ②若实验中用含有少量水的乙醇代替相同质量的无水 乙醇,相同条件下,测得的氢气体积将 水
[练习]
1.若要检验酒精中是否含有少量水,可选用的试剂是( )
(A)生石灰 (B)金属钠 (C)浓硫酸 (D)无水硫酸铜
2.制取无水酒精时,通常需向工业酒精中加入下列物质,并加热蒸馏,该物质是( ) (A)无水硫酸铜 (B)浓硫酸 (C)新制的生石灰 (D)碳化钙 3.下列物质发生化学反应,其化学反应类型属于加成反应又叫还原反应的是( ) (A)氢气和苯 (B)乙炔和氯化氢 (C)乙醇和浓硫酸 (D)甲烷和氯气 4.不能用加氢还原的方法得到的醇是( )
(A)C2H5OH (B)(CH3)3COH (C)(CH3)2CHOH (D)CH3OH
5.用硫酸酸化的CrO3遇酒精后,其颜色会从红色变为蓝绿色,用这个现象可以测得汽车司机是否酒后驾车。反应的化学方程式如下:
2CrO3+3C2H5OH+3H2SO4 == Cr2(SO4)3+3CH3CHO+6H2O
此反应的氧化剂是( )
(A)H2SO4 (B)CrO3 (C)Cr2(SO4)3 (D)C2H5OH
6.将W1 g光亮的铜丝在空气中加热一段时间后,迅速插入下列物质中,取出干燥,如此反复几次,最后取出铜丝用蒸馏水洗涤、干燥、称得其质量为W2 g。实验时由于所插入的物质不同,铜丝的前后质量变化可能不同,下列所插物质与铜丝的质量关系不正确的是( )
(A)石灰水W1 7.禁止用工业酒精配制饮料酒,这是因为工业酒精中常含有会使人中毒的( ) (A)乙醚 (B)乙二醇 (C)丙三醇 (D)甲醇 8.现有一瓶乙二醇和丙三醇的混和物,已知它们的性质如下表,据此,将乙二醇和丙三醇互相分离的最佳方法是( ) (C)分液法 (D)分馏法 (A)萃取法 (B)结晶法 苏教版化学必修2 共2页 第 2页 3/25/2013 6:56 PM 乙醇的结构简式为CH3CH2OH,俗称酒精,它在常温、常压下是一种易燃、易挥 发的无色透明液体,它的水溶液具有特殊的、令人愉快的香味,并略带刺激性。 乙醇的用途很广,可用乙醇来制造醋酸、饮料、香精、染料、燃料等。医疗上也 常用体积分数为70%——75%的乙醇作消毒剂等。 目录 引基本信息 性质 物理性质 化学性质 分类 用途 工业制法 危险性 引基本信息 性质 物理性质 化学性质 分类 用途 工业制法 危险性 , 吸收与代谢 , 包装与储运 , 泄漏处置和废弃 , 乙醇和甲醇的区别 , 乙醇密度表 , 健康 , 药物名称 展开 编辑本段引基本信息 中文名称: 乙醇 :又名 酒精 英文名称: ethyl alcohol ; etha 乙醇分子模型 nol ,fermentation alcohol, grain alcohol 分子式: C2H5OH 结构简式: CH3CH2OH或C2H5OH 官能团:羟基(-OH) CAS 登录号:64-17-5 EINECS 登录号:200-578-6 (结构如右图)C、O原子均以sp3杂化轨道成键、极性分子。 描述: 乙醇分子是由乙基和羟基两部分组成,可以看成是乙烷分子中的一个氢原子被羟基取代的产物,也可以看成是水分子中的一个氢原子被乙基取代的产物。乙醇分子中的碳氧键和氢氧键比较容易断裂。 相对分子量: 46.07 编辑本段性质 MolarMass = 46.06844(232) 乙醇 外观与性状: 无色液体,有特殊香味。 密度:0.789 g/cm^3; (液) 熔点:-114.3 ?C (158.8 K) 沸点:78.4 ?C (351.6 K) 在水中溶解时:pKa =15.9 黏度:1.200 mPa?s (cP), 20.0 ?C 分子偶极矩:5.64 fC?fm (1.69 D) (气) 折光率:1.3614 相对密度(水=1): 0.79 相对蒸气密度(空气=1): 1.59 饱和蒸气压(kPa): 5.33(19?) 燃烧热(kJ/mol): 1365.5 临界温度(?): 243.1 临界压力(MPa): 6.38 辛醇/水分配系数的对数值: 0.32 闪点(?): 12 引燃温度(?): 363 爆炸上限%(V/V): 19.0 爆炸下限%(V/V): 3.3 溶解性: 与水混溶,可混溶于醚、氯仿、甘油等多数有机溶剂。 电离性:非电解质 无色、透明,具有特殊香味的液体(易挥发),密度比水小,能跟水 以任意比互溶(一般不能做萃取剂)。是一种重要的溶剂,能溶解多种有 机物和无机物。 编辑本段物理性质 乙醇报警器 乙醇是一种很好的溶剂,既能溶解许多无机物,又能溶解许多有机物,所以常用乙醇来溶解植物色素或其中的药用成分,也常用乙醇作为反应的溶剂,使参加反应的有机物和无机物均能溶解,增大接触面积,提高反应速率。例如,在油脂的皂化反应中,加入乙醇既能溶解NaOH,又能溶解油脂,让它们在均相(同一溶剂的溶液)中充分接触,加快反应速率,提高反应限度。 乙醇的物理性质主要与 其低碳直链醇的性质有关。分子中的羟基可以形成氢键,因此乙醇黏度很大,也不及相近相对分子质量的有机化合物极性大。室温下,乙醇是无色易燃,且有特殊香味的挥发性液体。 λ=589.3nm和18.35?C下,乙醇的折射率为1.36242,比水稍高。 作为溶剂,乙醇易挥发,且可以与水、乙酸、丙酮、苯、四氯化碳、氯仿、乙醚、乙二醇、甘油、硝基甲烷、吡啶和甲苯等溶剂混溶。此外,低碳的脂肪族烃类如戊烷和己烷,氯代脂肪烃如1,1,1-三氯乙烷和四氯乙烯也可与乙醇混溶。随着碳数的增长,高碳醇在水中的溶解度明显下降。 由于存在氢键,乙醇具有潮解性,可以很快从空气中吸收水分。羟基的极性也使得很多离子化合物可溶于乙醇中,如氢氧化钠、氢氧化钾、氯化镁、氯化钙、氯化铵、溴化铵和溴化钠等。氯化钠和氯化钾则微溶于乙醇。此外,其非极性的烃基使得乙醇也可溶解一些非极性的物质,例如大多数香精油和很多增味剂、增色剂和医药试剂。 编辑本段化学性质 酸性 乙醇的各种化学式 ?乙醇分子中含有极化的氧氢键,电离时生成烷氧基负离子和质子。 CH3CH2OH?(可逆)CH3CH2O- + H+ 乙醇的pKa=15.9,与水相近。 乙醇的酸性很弱,但是电离平衡的存在足以使它与重水之间的同位素交换迅速进行。 CH3CH2OH+D2O?(可逆)CH3CH2OD+HOD 因为乙醇可以电离出极少量的氢离子,所以其只能与少量金属(主要是碱金属)反应生成对应的醇金属以及氢气: 2CH3CH2OH + 2Na?2CH3CH2ONa + H2? 乙醇可以和高活跃性金属反应,生成醇盐和氢气。 醇金属遇水则迅速水解生成醇和碱 结论: (1)乙醇可以与金属钠反应,产生氢气,但不如水与金属钠反应剧烈。 (2)活泼金属(钾、钙、钠、镁、铝)可以将乙醇羟基里的氢取代出来。 还原性 乙醇具有还原性,可以被氧化成为乙醛。酒精中毒的罪魁祸首通常被认为是有一定毒性的乙醛,而并非喝下去的乙醇。例如 2CH3CH2OH + O2 ? 2CH3CHO + 2H2O(条件是在催化剂Cu或Ag的作用下加热) 实际上是乙醇先和氧化铜进行反应,然后氧化铜被还原为单质铜,现象为:黑色氧化铜变成红色。 乙醇也可被高锰酸钾氧化,同时高锰酸钾由紫红色变为无色。乙醇也可以与酸性重铬酸钾溶液反应,当乙醇蒸汽进入含有酸性重铬酸钾溶液的硅胶中时,可见硅胶有橙红色变为草绿色,此反应现用于检验司机是否醉酒驾车。 酯化反应 乙醇可以与乙酸在浓硫酸的催化并加热的情况下发生酯化作用,生成乙酸乙酯(具有果香味)。 C2H5OH+CH3COOH,浓H2SO4?(可逆)?CH3COOCH2CH3+H2O(此为取代反 应) “酸”脱“羧基”,“醇”脱“羟基”上的“氢” 与氢卤酸反应 乙醇可以和卤化氢发生取代反应,生成卤代烃和水。 C2H5OH + HBr?C2H5Br + H2O或写成CH3CH2OH + HBr ? CH3CH2Br + H-OH C2H5OH + HX?C2H5X + H2O 注意:通常用溴化钠和硫酸的混合物与乙醇加热进行该反应。故常有红棕色气体产生。 氧化反应 (1)燃烧:发出淡蓝色火焰,生成二氧化碳和水(蒸气),并放出大量的热,不完全燃烧时还生成一氧化碳,有黄色火焰,放出热量 完全燃烧:C2H5OH+3O2?2CO2+3H2O (2)催化氧化:在加热和有催化剂(Cu或Ag)存在的情况下进行。 2Cu+O2,加热?2CuO C2H5OH+CuO?CH3CHO+Cu+H2O 即催化氧化的实质(用Cu作催化剂) 总式:2CH3CH2OH+O2,Cu或Ag?2CH3CHO+2H2O (工业制乙醛) 乙醇也可被浓硫酸跟高锰酸钾的混合物发生非常激烈的氧化反应,燃烧起来。(切记要注酸入醇,酸与醇的比例是1:3) 消去反应和脱水反应 乙醇可以在浓硫酸和高温的催化发生脱水反应,随着温度的不同生成物也不同。 (1)消去(分子内脱水)制乙烯(170?浓硫酸)制取时要在烧瓶中加入碎瓷片以免爆沸。 C2H5OH?CH2=CH2?+H2O (2)缩合(分子间脱水)制乙醚(130?-140? 浓硫酸) 2C2H5OH ?C2H5OC2H5 + H2O(此为取代反应) 药理作用 广泛用于医用消毒。一般使用 95%的酒精用于器械消毒;70~75%的酒精用于杀菌,例如 75%的酒精在常温(25C)下一分内可以杀死 大肠杆菌、金黄色葡萄球菌、白色念珠菌、白色念球菌、铜绿假单胞菌等;更低浓度的酒精用于降低体温,促进局部血液循环等。 乙醇还可以用于食用,如酒。因为它能作为良好的有机溶剂,所以中医用它来送服中药,以溶解中药中大部分有机成分。 编辑本段分类 (1)按生产使用的原料可分为淀粉质原料发酵酒精(一般有薯类、谷类和野生植物等含淀粉质的原料,在微生物作用下将淀粉水解为葡萄糖,再进一步由酵母发酵生成酒精);糖蜜原料发酵酒精(直接利用糖蜜中的糖分,经过稀释杀菌并添加部分营养盐,借酵母的作用发酵生成酒精);和亚硫酸盐纸浆废液发酵生产酒精(利用造纸废液中含有的六碳糖,在酵母作用下发酵成酒精,主要产品为工业用酒精。也有用木屑稀酸水解制作的酒精)。 (2)按生产的方法来分,可分为发酵法酒精和合成法酒精两大类。 (3)按产品质量或性质来分,又分为高纯度酒精、无水酒精、普通酒精和变性酒精。 (4)按产品系列(BG384-81)分为优级、一级、二级、三级和四级。其中一、二级相当于高纯度酒精及普通精馏酒精。三级相当于医药酒精,四级相当于工业酒精。新增二级标准是为了满足不同用户和生产的需要,减少生产与使用上的浪费,促进提高产品质量而制订的。 编辑本段用途 乙醇的用途很广,主要有: (1)不同浓度的消毒剂: 99.5,的酒精称为无水酒精。生物学中的用途:叶绿体中的色素能在有机溶剂无水乙醇(或丙酮)中,所以用无水乙醇可以提取叶绿体中的色素 95%的酒精用于擦拭紫外线灯。这种酒精在医院常用,而在家庭中则只会将其用于相机镜头的清洁。 70%,75%的酒精用于消毒。这是因为,过高浓度的酒精会在细菌表面形成一层保护膜,阻止其进入细菌体内,难以将细菌彻底杀死。若酒精浓度过低,虽可进入细菌,但不能将其体内的蛋白质凝固,同样也不能将细菌彻底杀死。其中70%的酒精消毒效果最好。 40%,50%的酒精可预防褥疮。长期卧床患者的背、腰、臀部因长期受压可引发褥疮,如按摩时将少许40%,50%的酒精倒入手中,均匀地按摩患者受压部位,就能达到促进局部血液循环,防止褥疮形成的目的。 25%,50%的酒精可用于物理退热。高烧患者可用其擦身,达到降温的目的。因为用酒精擦拭皮肤,能使患者的皮肤血管扩张,增加皮肤的散热能力,酒精蒸发,吸热,使病人体表面温度降低,症状缓解。但酒精浓度不可过高,否则可能会刺激皮肤,并吸收表皮大量的水分。 (2)饮料: 乙醇是酒主要成分(含量和酒的种类有关系)如白酒为56度的酒。注意:我们喝的酒内的乙醇不是把乙醇加进去,而是发酵出来的乙醇,当然根据使用的发酵酶不同还会有乙酸或糖等有关物质。 (3)基本有机化工原料: 乙醇可用来制取乙醛、乙醚、乙酸乙酯、乙胺等化工原料,也是制取、染料、涂料、洗涤剂等产品的原料 (4)汽车燃料: 乙醇可以调入汽油,作为车用燃料,我国雅津甜高粱乙醇在汽油中占10%。美国销售乙醇汽油已有20年历史。 此外乙醇还做:稀释剂、有机溶剂、涂料溶剂等几大方面,其中用量最大的是消毒剂。 编辑本段工业制法 工业上一般用淀粉发酵法或乙烯直接水化法制取乙醇: 1(发酵法 发酵法制乙醇是在酿酒的基础上发展起来的,在相当长的历史时期内,曾是生产乙醇的唯一工业方法。发酵法的原料可以是含淀粉的农产品,如谷类、薯类或野生植物果实等;也可用制糖厂的废糖蜜;或者用含纤维素的木屑、植物茎秆等。这些物质经一定的预处理后,经水解(用废蜜糖作原料部经这一步)、发酵,即可制得乙醇。 发酵液中的质量分数约为6%~10%,并含有其他一些有机杂质,经精馏可得95%的工业乙醇。 2(乙烯水化法 乙烯直接水化法,就是在加热、加压和有催化剂存在的条件下,是乙烯与水直接反应,生产乙醇: CH2?CH2 + H?OH?C2H5OH(该反应分两步进行,第一步是与醋酸汞等汞盐在水-四氢呋喃溶液中生成有机汞化合物,而后用硼氢化钠还原) 此法中的原料—乙烯可大量取自石油裂解气,成本低,产量大,这样能节约大量粮食,因此发展很快。 编辑本段危险性 EU分类 可燃 (F) 警示性质标准词 R11 安全建议标准词 S2, S7, S16 闪点 286.15 K (13 ?C or 55.4 ?F) 毒性:属微毒性。 急性毒性:LD507060mg/kg(兔经口);7340mg/kg(兔经皮);LC5037620mg/m3,10小时(大鼠吸入);人吸入4.3mg/L×50分钟,头面部发热,四肢发凉,头痛;人吸入2.6mg/L×39分钟,头痛,无后作用。 刺激性:家兔经眼:500mg,重度刺激。家兔经皮开放性刺激试验:15mg/24小时,轻度刺激。 亚急性和慢性毒性:大鼠经口10.2g/(kg?天),12周,体重下降,脂肪肝。 致突变性:微生物致突变:鼠伤寒沙门氏菌阴性。显性致死试验:小鼠经口1,1.5g/(kg?天),2周,阳性。 生殖毒性:大鼠腹腔最低中毒浓度(TDL0):7.5g/kg(孕9天),致畸阳性。 致癌性:小鼠经口最低中毒剂量(TDL0):340mg/kg(57周,间断),致癌阳性。 健康危害 本品为中枢神经系统抑制剂。首先引起兴奋,随后抑制。急性中毒:急性中毒多发生于口服。一般可分为兴奋、催眠、麻醉、窒息四阶段。患者进入第三或第四阶段,出现意识丧失、瞳孔扩大、呼吸不规律、休克、心力循环衰竭及呼吸停止。慢性影响:在生产中长期接触高浓度本品可引起鼻、眼、粘膜刺激症状,以及头痛、头晕、疲乏、易激动、震颤、恶心等。长期酗酒可引起多发性神经病、慢性胃炎、脂肪肝、肝硬化、心肌损害及器质性精神病等。皮肤长期接触可引起干燥、脱屑、皲裂和皮炎。 乙醇具有成瘾性及致癌性,但乙醇并不是直接导致癌症的物质,而是致癌物质普遍溶于乙醇。在中国传统医药观点上,乙醇有促进人体吸收药物的功能,并能促进血液循环,治疗虚冷症状。药酒便是依照此原理制备出来的。 燃爆危险: 本品易燃,具刺激性。 危险特性: 易燃,其蒸气与空气可形成爆炸性混合物,遇明火、高热能引起燃烧爆炸。与氧化剂接触发生化学反应或引起燃烧。在火场中,受热的容器有爆炸危险。其蒸气比空气重,能在较低处扩散到相当远的地方,遇火源会着火回燃。 急救: 皮肤接触: 脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。 眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。就医。 吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼吸。就医。 食入: 饮足量温水,催吐。就医。 防护措施 工程控制: 密闭操作,加强通风 呼吸系统防护: 空气中浓度较高时,应该佩戴自吸过滤式防尘口罩。必要时,建议佩戴自给式呼吸器 眼睛防护: 戴化学安全防护眼镜。 身体防护: 穿胶布防毒衣。 手防护: 戴橡胶手套。 其他防护: 工作完毕,淋浴更衣。保持良好的卫生习惯。 编辑本段吸收与代谢 乙醇的吸收: 饮酒后,乙醇很快通过胃和小肠的毛细血管进入血液。一般情况下,饮酒者血液中乙醇的浓度(blood alcohol concentration,BAC)在30~45分钟内将达到最大值,随后逐渐降低。当BAC超过1000mg/L时,将可能引起明显的乙醇中毒。摄入体内的乙醇除少量未被代谢而通过呼吸和尿液直接排出外,大部分乙醇需被氧化分解。 乙醇的代谢: 在乙醇的代谢过程中乙醇脱氢酶(alcohol dehydrogenase,ADH)起着至关重要的作用,它主要分布在肝脏,在胃肠道及其他组织中也有少量分布。乙醇通过血液流到肝脏后,首先被ADH氧化为乙醛,而乙醛脱氢酶则能把乙醛中的两个氢原子脱掉,分解为二氧化碳和水,在肝脏中乙醇还能被CYP2E1酶分解代谢。 人喝酒后面部潮红,是因为皮下暂时性血管扩张所致,因为这些人体内有高效的乙醇脱氢酶,能迅速将血液中的酒精转化成乙醛,而乙醛具有让毛细血管扩张的功能,会引起脸色泛红甚至身上皮肤潮红等现象,也就是我们平时所说的“上脸”。 乙醇代谢的速率主要取决于体内酶的含量,其具有较大的个体差异,并与遗传有关。人体内若是具备这两种酶,就能较快地分解酒精,中枢神经就较少受到酒精的作用,因而即使喝了一定量的酒后,也行若无事。在 人体中,都存在乙醇脱氢酶,而且大部分人数量基本是相等的。但缺少乙醛脱氢酶的人就比较多。这种乙醛脱氢酶的缺少,使酒精不能被完全分解为水和二氧化碳,而是以乙醛继续留在体内。你所说的酒精的代谢应该是被完整的分解后的状态,由于很多人缺少乙醛脱氢酶,拥有乙醛脱氢酶的量也是有差别的,所以严格的说酒精的代谢速度是没法用一个准确的速度来描述的,因人而异。 编辑本段包装与储运 包装方法: 两层塑料袋或一层塑料袋外麻袋、塑料编织袋、乳胶布袋;塑料袋外复合塑料编织袋(聚丙烯三合一袋、聚乙烯三合一袋、聚丙烯二合一袋、聚乙烯二合一袋);螺纹口玻璃瓶、铁盖压口玻璃瓶、塑料瓶或金属桶(罐)外普通木箱;螺纹口玻璃瓶、塑料瓶或镀锡薄钢板桶(罐)外满底板花格箱、纤维板箱或胶合板箱。 小开口钢桶;小开口铝桶;螺纹口玻璃瓶、铁盖压口玻璃瓶、塑料瓶或金属桶(罐)外木板箱。 危规号: 32061 UN编号: 1170 包装类别: O53;?类 包装标志: 易燃品;7 储运注意事项: 铁路运输时应严格按照铁道部《危险货物运输规则》中的危险货物配装表进行配装。运输时单独装运,运输过程中要确保容器不泄漏、不倒塌、不坠落、不损坏。运输时运输车辆应配备相应品种和数量的消防器材。严禁与酸类、易燃物、有机物、还原剂、自燃物品、遇湿易燃物品等并车混运。运输时车速不宜过快,不得强行超车。运输车辆装卸前后,均应彻底清扫、洗净,严禁混入有机物。储存于阴凉、通风的库房。远离火种、热 源。库温不超过30?,相对湿度不超过80,。包装要求密封,不可与空气接触。应与还原剂、活性金属粉末、酸类、食用化学品分开存放,切忌混储。储区应备有合适的材料收容泄漏物。 储存于阴凉、通风仓间内。远离火种、热源。仓内温度不宜超过30?。防止阳光直射。保持容器密封。应与氧化剂分开存放。储存间内的照明、通风等设施应采用防爆型,开关设在仓外。配备相应品种和数量的消防器材。桶装堆垛不可过大,应留墙距、顶距、柱距及必要的防火检查走道。储罐时要有防火防爆技术措施。露天储罐夏季要有降温措施。禁止使用易产生火花的机械设备和工具。灌装时应注意流速(不超过3m/s),且有接地装置,防止静电积聚。 编辑本段泄漏处置和废弃 泄漏处置方法: 隔离泄漏污染区,限制出入。建议应急处理人员戴防尘面具(全面罩),穿防毒服。勿使泄漏物与还原剂、有机物、易燃物或金属粉末接触。不要直接接触泄漏物。小量泄漏:用洁净的铲子收集于干燥、洁净、有盖的容器中。大量泄漏就收集回收或运至废物处理场所处置。 废弃方法: 根据国家和地方有关法规的要求处置。或与厂商或制造商联系,确定处置方法。 编辑本段乙醇和甲醇的区别 甲醇是甲烷的一个氢原子被羟基(一个氢和一个氧组成的原子团,不是氢氧根)替换后的产物。 乙醇是乙烷一个氢原子被羟基替换后的产物,俗称酒精。 分子式不一样。 甲烷:CH4 甲醇:CH3OH 乙醇:CH3CH2OH 乙醇结构 甲醇结构 他们的分子式不一样,化学性质和物理性质也有区别。 编辑本段乙醇密度表 乙醇溶液密度(g/cm3)(20?)-每(g/cm3)含有乙醇重量(%)g-浓度 (体积比%)=度(1度=1%体积) 0.998-0.15-0.2 0.996-1.20-1.5 0.994-2.30-3.0 0.992-3.50-4.4 0.990-4.70-5.9 0.988-5.90-7.4 0.985-7.90-9.9 0.982-10.0-12.5 0.980-11.5-14.2 0.978-13.0-16.0 0.975-15.3-18.9 0.972-17.6-21.7 0.970-19.1-23.5 0.968-20.6-25.3 0.965-22.8-27.8 0.962-24.8-30.3 0.960-26.2-31.8 0.957-28.1-34.0 0.954-29.9-36.1 0.950-32.2-38.8 0.945-35.0-41.3 0.940-37.6-44.8 0.935-40.1-47.5 0.930-42.6-50.2 0.925-44.9-52.7 0.920-47.3-55.1 0.915-49.5-57.4 0.910-51.8-59.7 0.905-53.9-61.9 0.900-56.2-64.0 0.895-58.3-66.2 0.890-60.5-68.2 0.885-62.7-70.2 0.880-64.8-72.2 0.875-66.9-74.2 0.870-69.0-76.1 0.865-71.1-77.9 0.860-73.2-79.7 0.855-75.3-81.5 0.850-77.3-83.3 0.845-79.4-85.0 0.840-81.4-86.6 0.835-83.4-88.2 0.830-85.4-89.8 0.825-87.3-91.2 0.820-89.2-92.7 0.815-91.1-94.1 0.810-93.0-95.4 0.805-94.4-96.6 0.800-96.5-97.7 0.795-98.2-98.9 0.791-99.5-99.7 从中可以计算出:每(g/cm3)含有乙醇重量(%)g 浓度(体积比%)=度(1度=1%体积) 例如:密度为0.791g/cm3 每(g/cm3)含有乙醇重量:0.791×99.5%=0.787045g 浓度:99.7%=99.7度 编辑本段健康 酒精(乙醇)具有成瘾性及致癌性,但乙醇并不是直接导致癌症的物 质,而是致癌物质普遍溶于乙醇。在中国传统医药观点上,乙醇有促进人 体吸收药物的功能,并能促进血液循环,治疗虚冷症状。药酒便是依照此 原理制备出来的。 漱口水如果含有较高浓度的酒精,就算不吞入也可能有害健康。 编辑本段药物名称 中文名:乙醇 拼音名:yǐ chun 英文名:Alcohol 书页号:2000年版二部,11 C2H6O 46.07 【性状】 本品为无色澄明液体;微有特臭,味灼烈;易挥发,易燃烧,燃烧时显 淡蓝色火焰;热至约78?即沸腾。 本品与水、甘油、氯仿或乙醚能任意混溶。 相对密度 本品的相对密度(附录? A)不大于0.8129,相当于含C2H6O 不少于 95.0,(ml,ml)。 【鉴别】 取本品1ml ,加水5ml 与氢氧化钠试液1ml 后,缓缓滴加碘试液2ml , 即发生碘仿的臭气,并生成黄色沉淀。 【检查】 酸度 取本品10ml,加水25ml及酚酞指示液2 滴,摇匀,滴加氢氧化钠 滴定液(0.02mol/L) 至显淡红色,再加本品25ml,摇匀,加氢氧化钠滴定液(0.02mol/L )0.50ml,应显淡红色。 水不溶性物质 取本品,与同体积的水混合后,溶液应澄清;在10?放置30分钟, 溶液仍应澄清。 杂醇油 取本品10ml,加水5ml 与甘油1ml ,摇匀后,分次滴加在无臭的滤纸上, 使乙醇自然挥散,始终不得发生异臭。 甲醇 取本品5ml ,用水稀释至100ml ,摇匀;分取 1.0ml,加磷酸溶液(1?10) 0.2ml 与5,高锰酸钾溶液0.25ml,在30,35?保温15分钟,滴加10,焦亚硫酸钠溶液 至无色,缓缓加入在冰浴中冷却的硫酸溶液(3?4)5ml ,在加入时应保持混合物冷却; 再加新制的1,变色酸溶液0.1ml,置水浴中加热20分钟,如显色,与标准甲醇溶液(精 密称取甲醇20mg,加水使成200ml )1.0ml 用同一方法制成的对照液比较,不得更深( 0.20,)。 易氧化物 取50ml具塞量筒,依次用盐酸、水与本品洗净后,加入本品20ml,放冷 至15?,加高锰酸钾滴定液(0.02mol/L)0.10ml ,密塞摇匀后,在15?静置10分钟,粉 红色不得完全消失。 丙酮和异丙醇 取本品1.0ml ,加水1.0ml 、磷酸氢二钠的饱和溶液1.0ml 与高锰 酸钾的饱和溶液3.0ml ,混匀后,置45,50?水浴中,待高锰酸钾褪色后,加10,氢氧 化钠溶液3.0ml ,摇匀,用垂熔玻璃漏斗滤过,滤液中加新制的1,糠醛溶液1.0ml , 放置10分钟后,取出1.0ml ,加盐酸3.0ml ,在3 分钟内观察;如显粉红色,与对照液 (取磷酸氢二钠的饱和溶液1.0ml 、10,氢氧化钠溶液3.0ml 与0.001 ,丙酮溶液 0.8 ml,加1 ,糠醛溶液1.0ml,用水稀释成10ml,放置10分钟后,取出1.0ml,加盐酸3.0ml )比较,不得更深(0.0008,)。 戊醇或不挥发的易炭化物 取本品25ml,置蒸发皿中,于水浴上蒸发至器皿表面微 显湿润(约剩0.05ml),加95,硫酸数滴,不得染成红色或棕色。 不挥发物 取本品40ml,置105?恒重的蒸发皿中,于水浴上蒸干后,在105?干燥 2小时,遗留残渣不得过1mg。 【类别】 消毒防腐药、溶剂。 【贮藏】 遮光,密封保存。范文五:乙醇的结构简式为CH3CH2OH



 雘籭檷墢欛
雘籭檷墢欛

