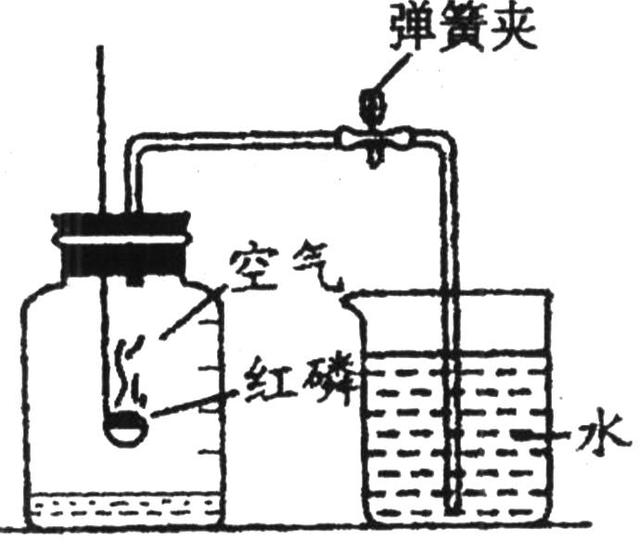
范文一:演示实验:空气的成分
姓名:______________
空氣的組成 座號:______________
日期:______________
一、 演示實驗:空氣的成分
1. 保特瓶內沒有鋼絲絨時,插入的線香會繼續燃燒,表示裡面還
有【 】。
2. 保特瓶加入鋼絲絨以後,瓶口加蓋,插入的線香不會繼續燃燒,
表示瓶內的氧氣已經消耗完,以致於水面上升,上升體積大約
佔保特瓶【 】。
3. 保特瓶中殘餘的氣體不能像氧氣一樣幫助燃燒,可見是不一樣
的物質,所以空氣是由不同氣體所組成的【 】。
二、 空氣中主要的成分
1. 【 】約占78%:體積百分比:,其次是【 】。第三位是
【 】,三者皆為無色、無臭、無味的氣體。
4. 空氣中的【 】、【 】、【臭氧】等氣體,其所占
有的比例會因地點不同而有所改變。
5. 其他氣體包含亞氣、氩氣、氖氣等惰性氣體以及塵埃、微生物
或汙染物。
三、 氮
1. 無色、無臭、無味的氣體,不可燃也不助燃。
2. 室溫下幾乎不發生任何反映,但高溫時可與金屬或非金屬反應。 3. 主要用途::I:植物所須要的【 】。:?:工業上製造氨
或硝酸的原料。:?:食品包裝中抽出空氣,填充【 】可
保新鮮。:?:液態氮是良好的冷卻劑。
四、 氧
1. 無色、無臭、無味的氣體,能【 】但不可燃。 2. 活性大易與其他物質發生氧化反應,如:燃燒、生銹。 3. 生物呼吸、物質燃燒所必需之物。
五、 惰性氣體:不可燃也不助燃,高溫也不易反應,但用途極廣,又稱為【 】或【稀有氣體】。
1. 氩:密度比空氣小,很不活潑,可代替【 】填充飛行氣球。 2. 氖:裝入燈管,通電時會發出紅光,可以做為霓虹燈或信號燈。 3. 亞:焊接金屬時,可以防止金屬與【 】反應。另外,在
燈泡中充入亞氣可以防止燈絲氧化。
范文二:空气成分实验改进 空气组成测定实验的改进
摘要:针对初三《化学》中“空气中氧气体积含量的测定”实验存在的不足进行了改进,并对改进后设计的实验进行反思。关键词:氧气含量测定;实验改进;反思文章编号:1005,6629(2009)03,0015,03中图分类号:G633.8文献标识码:C1问题的…
文章编号:1005,6629(2009)03,0014,02中图分类号:G633.8文献标识码:C2007年1月人教版全日制普通高级中学教科书(必修加选修)化学第二册P72[实验4-4]铝热反应实验装置,是沿用了20多年的传统实验装置,在多年的实验教…
摘要:运用塑料罩和氢氧化钠溶液可减少蔗糖与浓硫酸脱水反应的演示实验的污染,让学生在雾中欣赏鲜花的变色,增强实验的趣味性。关键词:蔗糖;浓硫酸;实验改进文章编号:1005,6629(2009)03,0013,02中图分类号:G633.8文献标识码:C蔗…
1
摘要:针对初三《化学》中“空气中氧气体积含量的测定”实验存在的不足进行了改进,并对改进后设计的实验进行反思。
关键词:氧气含量测定; 实验改进; 反思
文章编号:1005,6629(2009)03,0015,03中图分类号:G633.8文献标识码:C
1 问题的提出
沪教版九年级《化学》(2004年5月第二版)上册第27页图2-1(如图1)“空气中氧气体积含量的测定”实验,其原理是通过燃着的红磷伸入广口瓶中密闭燃烧的方法测定空气中氧气的含量。该实验特别强调装置的气密性、红磷用量、冷却到室温后才能打开止水夹等因素,但除此之外在实际操作中,还存在下列问题:用酒精灯点燃红磷时,不可避免有少量五氧化二磷污染环境;导管中存有空气;将盛有燃着的红磷的燃烧匙伸入到集气瓶时易产生少量热空气外逸;有时为了追求燃烧匙伸入到集气瓶中的速度,还会出现火焰熄灭、停止燃烧的现象。
为了进一步完善教材中的实验方案,提高实验的科学
2
性、准确性,笔者对此实验进行了改进探究,借鉴同行们一些好的做法和想法,现列举如下4种改进方法,并反思其中的优点与不足,旨在能“抛砖引玉”。
2 实验改进
2(1改进点燃手段
(1)案例一:水浴引燃法
如图2所示,将教材中带有刻度的集气瓶改为锥形瓶,烧杯改为注射器,红磷改为白磷。实验前先将锥形瓶中装满水,用量筒测量出锥形瓶的容积,再将白磷放入干燥的锥形瓶中,夹紧止水夹,注射器中盛放一定量的红墨水,水浴加热锥形瓶,待白磷燃烧熄灭后冷却至室温,打开止水夹,读出注射器内红墨水减少的体积数。
该装置的优点有:?避免了锥形瓶中空气受热膨胀在密闭前外逸;?白磷在密闭的环境中点燃,无污染。但也存在不足:导管内存有空气,影响实验测定的准确性。
(2)案例二:电热引燃法
如图3所示,将用酒精灯加热改为电源加热,通过测量a、b、c三个数据得出结论。实验前先在集气瓶里装进a
3
体积的水,燃烧匙里放一块白磷,将导管的另一端放入盛有足量水的烧杯中(注:集气瓶内的长导管伸到瓶底)。接通电源片刻,观察到白磷立即着火燃烧,关闭电源,观察到产生大量白烟,同时放出大量的热。待白磷燃烧熄灭后,稍加振荡,白烟消失,待集气瓶完全冷却至室温,量出集气瓶中水的体积是b(整个集气瓶的体积是c)。
该装置的优点有:?白磷在密闭容器中点燃,不会造成污染环境;?避免了集气瓶中空气受热膨胀在密闭前外逸;?用电源引燃比较方便;?集气瓶冷却速度较快,可节省实验时间。但存在的不足是:?导管内仍存有空气,影响实验的准确性;?难以精确测量a、b、c三个数值。
2(2排除导管空气
(1)案例一:引入注射器
如图4所示,在图2方法的基础上,将注射器改为装有100mL水的量筒,锥形瓶改为集气瓶,单孔瓶塞改为双孔瓶塞。实验前先塞紧瓶塞,打开止水夹k1、k2,稍稍拉动注射器的栓塞,使得右侧的导管里充满水,然后关闭k1、k2。打开瓶塞,将吸进集气瓶中的水倒入量筒中,将燃烧匙内装有足量的白磷。引燃白磷,待白磷燃烧熄灭后冷却至室温,打开止水夹k2,读出量筒内剩余水的体积数。
该装置的优点有:?排除了右侧导管内存有的空气,
4
精确程度相对稍高一些;?避免了集气瓶中空气受热膨胀在密闭前外逸;?白磷在密闭的环境中点燃,无污染。存在的不足是:左侧连接注射器的导管内仍存有空气,影响实验的准确性。
(2)案例二:引用吸滤瓶
将集气瓶改为吸滤瓶(如图5),在吸滤瓶的支管上连接注射器。实验前先在量筒里装有100mL的水,打开止水夹k1、k2,稍稍拉动注射器的栓塞,使得右侧的导管里充满水,然后关闭k1、k2。打开瓶塞,把吸进吸滤瓶中的水倒入量筒中,在燃烧匙内放入过量的红磷,再放入1颗黄豆粒大的白磷,用白磷引燃红磷。待红磷燃烧熄灭后冷却至室温,打开止水夹k2,读出量筒内剩余水的体积数。
该装置的优点有:?吸滤瓶内的气体不会因受热膨胀而逸出;?排除了导管内存有的空气,提高了实验的准确性;?红磷在密闭容器中引燃,不会造成污染环境。存在的不足是:右侧的导管里充满水后打开瓶塞时,操作上不太方便。
3 讨论与反思
化学实验的改进是一项长期、艰巨而具有深远意义的工程,其中有许多方面值得探究和挖掘。实验改进不可能有
5
一个固定的模式,我们只要做一个有心人,把平时教学过程中针对某一实验问题的突发灵感或巧妙构想进行日积月累,就逐渐会从实验操作者变为实验创新者。一个实验完美无缺的改进方案是极少见的,尽管我们花费了很多心血和努力,缺陷或不足仍然在所难免。如:空气组成的探究实验在中学化学实验教学中,经历了从简单定量到精确定量的过程,研究的主要焦点是:药品使用、点燃方式探讨、导管中空气的排除等。由于受到诸多条件的制约,无论从哪方面改,得到结论的精确程度也只能是相对的,改进后的任何一套方案也许是“仁者见仁,智者见智”。像关于白磷代替红磷的问题,白磷虽然着火点低,易引燃,但白磷有剧毒。还有的改进方案中设想,用木炭代替红磷,将水改为氢氧化钠溶液,但实际的情况也很复杂,木炭块的大小、加热燃烧的程度等都是影响实验结果的因素,并且木炭在密闭的容器中燃烧,不仅很难将氧气耗尽,而且还会产生少量的一氧化碳气体。所以我们从实验改进中跳出来看,不难发现,追求改进的“过程”比获得精确的结论更为重要,实验改进经历了思考、探究、创新的过程,从本质上说是一种追求学生化学素养提升的过程,从实验教学的另一个纬度锻炼了学生的思维能力,促进了学生的有意义学习,这正是我们今天倡导化学实验改进的精髓所在。
6
摘要:针对初三《化学》中“空气中氧气体积含量的测定”实验存在的不足进行了改进,并对改进后设计的实验进行反思。关键词:氧气含量测定;实验改进;反思文章编号:1005,6629(2009)03,0015,03中图分类号:G633.8文献标识码:C1问题的…
摘要:针对初三《化学》中“空气中氧气体积含量的测定”实验存在的不足进行了改进,并对改进后设计的实验进行反思。关键词:氧气含量测定;实验改进;反思文章编号:1005,6629(2009)03,0015,03中图分类号:G633.8文献标识码:C1问题的…
摘要:针对初三《化学》中“空气中氧气体积含量的测定”实验存在的不足进行了改进,并对改进后设计的实验进行反思。关键词:氧气含量测定;实验改进;反思文章编号:1005,6629(2009)03,0015,03中图分类号:G633.8文献标识码:C1问题的…
百度搜索“就爱阅读”,专业资料,生活学习,尽在就爱阅读网92to.com,您的在线图书馆
7
8
范文三:有关空气成分的测定实验例析
有关空气成分的测定实验例析
一、利用加热密闭容器内的物质消耗氧气测定空气中氧气的含量
[测定原理]利用某些物质在加热的条件下能与氧气反应的性质,消耗密闭容器内的氧气,容器内气体减少的量即是氧气的量。
例1.小红和小明分别用如图所示的装置测定空气中氧气的含量,玻璃管内装有细铜丝,且注射器的密闭系统内留有30 mL室温下的空气。
[问题]1.如果他们的实验很成功,出现的现象是:
细铜丝由________色变为________色,冷却后,密闭
容器内气体的体积约为_________mL。
3.小明发现自己测出的氧气的体积分数偏小,请你帮他分析一下原因。
[解析]本实验是利用加热细铜丝消耗密闭容器内的氧气而不产生新的气体,冷却后,密闭容器体积减少的量即为氧气的体积。由于氧气的体积约占空气体积的1/5,原有空气30 mL,氧气约为6 mL,剩余24 mL。此实验一定要使容器内所有的氧气都参加反应,并且装置不漏气,硬质玻璃管要冷却到室温,否则实验结果会偏小。
[答案]1. 红;黑;24 2.①细铜丝的量不足;②装置的气密性不好;③加热的时间较短、温度较低;④装置未冷却就读数;
二、利用可燃物燃烧消耗氧气测定空气中氧气的含量
[测定原理]利用物质燃烧消耗密闭容器内空气中的氧气,使密闭容器内气体的压强减小,在大气压的作用下,进入容器内水的体积即为减少的氧气的体积。
例2在“空气中氧气含量的测定”实验探究中,甲生设计了如下实验方案:
在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶。(实验装置如下图所示)回答下列问题: (1)实验过程中,观察到的主要现象是 , 。
(2)乙生用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏差,其操作上的原因可能是 (要求答出两种)。
(3)丙生也设计了一个实验方案,装置和操作同上,只不过用木炭代替了红磷。当木炭停止燃烧,集气瓶冷却至室温,打开铁夹后,水能否进入集气瓶?为什么?
(4)若仍然用木炭代替红磷,丙生的实验方案应作何改进,才能保证实验成功?(只需答出实验方案中须改进的地方)
[解析]解答此类题目应注意可燃物的选择应满足:(1)该物质在空气中可以燃烧且只与空气中的氧气反应;(2)燃烧后不能有气体生成或生成的气体可以完全溶于实验所用的液体;(3)所选可燃物必须足量。
[答案] (1)红磷燃烧生成大量白烟 进入集气瓶中的水约占其体积的1/5
(2)瓶塞未塞紧,造成装置漏气; 红磷不足; 集气瓶未冷却至室温就打开铁夹
(3)不能,木炭燃烧生成的CO2与消耗的氧气体积相等,使燃烧前后集气瓶内压强不变。
(4)在集气瓶内壁上预先注入少量氢氧化钠溶液;或在瓶塞上插入吸有NaOH溶液的胶头滴管,在打开铁夹前,将胶头滴管中的NaOH溶液注入集气瓶中。
同步练习
1.某同学用下图所示的装置粗略地测定空气中氧气的体积分数。图中烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,活塞左端管内密封有常温下的空气和白磷,已知当温度达到40℃时白磷能够在空气中燃烧。活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度 5 cm 处。
( 1 )向烧杯内加入适量水,与生石灰反应的目的是 _____________ 。
( 2 )可观察到玻璃管内开始发生的现象为:①白磷(足量) _____________ ;②活塞向(填左、右) _____________ 移动。
( 3 )实验结束,恢复至常温,活塞应停在约 _____________cm 处,据此可得出的结论是 _____________ 。
第1题图 第2题图
2.如图所示,将一端螺旋状的铜丝封在试管内用酒精灯加热足够的时间。
(1)未加热时,铜丝呈____色,加热一段时间后呈___色,反应的文字表达式 。
(2)停止加热。冷却到室温打开止水夹,烧杯内的水会________,大约达到试管体积的_______为止。
(3)此实验说明,试管内含有______,大约占________,剩余气体中若放一小虫,小虫会___________,这是因为_____________________________________。
空气中氧气含量的测定是利用氧气易跟其他物质发生反应的性质,在密闭容器中燃烧某种物质,使其中的氧气被消耗掉,根据气体体积的变化判断氧气的含量。因此,确保这类实验成功的关键是:①所选用的物质须是可以与氧气发生反应而不和空气中的其它成分发生反应的物质;②所选用的物质须为固体;③生成物应为固体,或者生成的气体极易溶于水或能被某种液体吸收;④装置的气密性要好;⑤所选物质须足量,以保证装置内氧气被完全消耗掉;⑥实验结束时,须等到装置冷却至室温再开始读数。下面介绍两种测定空气中氧气含量的实验方法。
范文四:空气成分测定实验的改进
空气成分测定实验的改进
一、 问题的提出
化学是一门以实验为基础的科学。演示实验的成败与效果不仅影响学生对化学知识的理解掌握情况,还直接影响着学生的学习情绪及对化学的兴趣。演示实验“用时短、现象明显、易于观察”,则学生学习化学的兴趣大增,情绪高涨,课堂气氛活跃,教学效果良好;反之,则学生情绪低沉,实验的失败直接导致教学的失败。原初三化学教材与现行九年级化学新课程中对空气成分的测定实验设置,分别在钟罩或集气瓶内进行,虽略有不同,但都达不到理想的实验效果。主要存在以下问题:
1、反应容器不规则,难以等分。
2、反应容器较大,不但浪费药品,而且产生的热量多,系统冷却需要时间长(一般达20分钟以上),严重影响教学效率。
3、反应后水面一般达不到理想的上升高度。
二、实验改进
用原教材或新课程所设置的两种实验装置演示探索空气成分,由于反应容器过大,空气量多,燃烧时间长,产生热量多,系统不易冷却,既费药品又费时间;另为,水面上升高度也不理想。若将实验改在玻璃管中进行,并利用投影辅助教学,便能收到良好的效果。
1、仪器、药品:投影仪、玻璃管(用底部破损的大试管代替)、
橡皮带、橡皮塞、铁架台、酒精灯、火柴、燃烧匙、药匙、红磷。
2、实验装置、步骤及现象
(1)如图:
将玻璃管(橡皮塞以下部分套5个橡皮带,并使间隔相等)伸入盛水(水中滴几滴红墨水)的烧杯中,并用铁架台固定。
(2)在小燃烧匙 (或费旧燃烧
匙改装小,以便能插入玻璃管)盛少量红磷,用酒精灯点燃后立即插入玻璃管内,然后塞紧所配的橡皮塞,观察红磷的燃烧和水面变化的情况;同时利用投影辅助观察。
(3)可以看到红磷燃烧时有大量白烟生成,同时玻璃管内水面明显上升。片刻后燃烧的红磷熄灭,过一会儿,白烟消失,玻璃管内水面上升到略高于第二个(从下往上)橡皮带处。
三、改进的优点
实验在玻璃管中进行演示,不但能使水面上升到理想的高度,同时由于水面上升幅度大,加之水中加入红墨水、玻璃管上套有橡皮带,并利用投影辅助教学,便于学生观察;还能节省药品和时间。符合演示实验“用时短、现象明显、易于观察”的要求。从而达到良好的教学效果。
有关空气成分的测定实验例析
作者:济南 曲文… 文章来源:转载 点击数:2481 更新时间:2007-10-4
空气中氧气含量的测定是利用氧气易跟其他物质发生反应的性质,在密闭容器中燃烧某种物质,使其中的氧气被消耗掉, 根据气体体积的变化判断氧气的含量。因此,确保这类实验成功的关键是:?所选用的物质须是可以与氧气发生反应而不和空气中的其它成分发生反应的物质;?所选用的物质须为固体;?生成物应为固体,或者生成的气体极易溶于水或能被某种液体吸收;?装置的气密性要好;?所选物质须足量,以保证装置内氧气被完全消耗掉;?实验结束时,须等到装置冷却至室温再开始读数。下面介绍两种测定空气中氧气含量的实验方法。
一、利用加热密闭容器内的物质消耗氧气测定空气中氧气的含量
[测定原理]利用某些物质在加热的条件下能与氧气反应的性质,消耗密闭容器内的氧气,容器内气体减少的量即是氧气的量。 例1(小红和小明分别用如图所示的装置测定空气中氧气的含量,硬质玻璃管内装有细铜丝,且两个注射器组成的密闭系统内留有30 mL室温下的空气。
[问题]1(如果他们的实验很成功,出现的现象是:
细铜丝由________色变为________色,冷却后,密闭
容器内气体的体积约为_________mL。
2(小红在做实验时,发现橡皮管被烤焦了,请你
帮他分析一下原因__________________________ 。
3(小明发现自己测出的氧气的体积分数偏小,请你帮他分析一下原因。
[解析]本实验是利用加热细铜丝消耗密闭容器内的氧气而不产生新的气体,冷却后,密闭容器体积减少的量即为氧气的体积。由于氧气的体积约占空气体积的1/5,原有空气30 mL,氧气约为6 mL,剩余24 mL。此实验一定要使容器内所有的氧气都参加反应,并且装置不漏气,硬质玻璃管要冷却到室温,否则实验结果会偏小。
[答案]1. 红;黑;24 2.硬质玻璃管太短、太细 3.?细铜丝的量不足;?装置的气密性不好;?加热的时间较短、温度较低;?装置未冷却就读数;?未将气体推至一只注射器,只读了一只中的数值。
二、利用可燃物燃烧消耗氧气测定空气中氧气的含量
[测定原理]利用物质燃烧消耗密闭容器内空气中的氧气,使密闭容器内气体的压强减小,在大气压的作用下,进入容器内水的体积即为减少的氧气的体积。
例2在“空气中氧气含量的测定”实验探究中,甲生设计了如下实验方案:
在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶。(实验装置如下图所示)回答下列问题:
(1)实验过程中,观察到的主要现象是 , 。
(2)乙生用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏差,其操作上的原因可能是
(要求答出两种)。
(3)丙生也设计了一个实验方案,装置和操作同上,只不过用木炭代替了红磷。当木炭停止燃烧,集气瓶冷却至室温,打开铁夹后,水能否进入集气瓶,为什么,
(4)若仍然用木炭代替红磷,丙生的实验方案应作何改进,才能保证实验成功,(只需答出实验方案中须改进的地方)
[解析]解答此类题目应注意可燃物的选择应满足:(1)该物质在空气中可以燃烧且只与空气中的氧气反应;(2)燃烧后不能有气体生成或生成的气体可以完全溶于实验所用的液体;(3)所选可燃物必须足量。
[答案] (1)红磷燃烧生成大量白烟 进入集气瓶中的水约占其体积的1/5
(2)瓶塞未塞紧,造成装置漏气; 红磷不足; 集气瓶未冷却至室温就打开铁夹
(3)不能,木炭燃烧生成的CO2与消耗的氧气体积相等,使燃烧前后集气瓶内压强不变。
(4)在集气瓶内壁上预先注入少量氢氧化钠溶液;或在瓶塞上插入吸有NaOH溶液的胶头滴管,在打开铁夹前,将胶头滴管中的NaOH溶液注入集气瓶中。
同步练习
1(某同学用下图所示的装置粗略地测定空气中氧气的体积分数。图中烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,活塞左端管内密封有常温下的空气和白磷,已知当温度达到,,?时白磷能够在空气中燃烧。活塞右端的玻璃管口跟空气连通,实验开始前活塞处在刻度 5 cm 处。
( 1 )向烧杯内加入适量水,与生石灰反应的目的是 _____________ 。
( 2 )可观察到玻璃管内开始发生的现象为:?白磷(足量) _____________ ;?活塞向(填左、右) _____________ 移动。
( 3 )实验结束,恢复至常温,活塞应停在约 _____________cm 处,据此可得出的结论是 _____________ 。
第1题图 第2题图
2.如图所示,将一端螺旋状的铜丝封在试管内用酒精灯加热足够的时间。
(1)未加热时,铜丝呈____色,加热一段时间后呈___色,反应的文字表达式 。
(2)停止加热。冷却到室温打开止水夹,烧杯内的水会________,大约达到试管体积的_______为止。 (3)此实验说明,试管内含有______,大约占________,剩余气体中若放一小虫,小虫会___________,这是因为_____________________________________。
空气成分测量(实验改进)
作者:白福秦 文章来源:《实验教师培训教程》 点击数:809 更新时间:2007-8-22
有关空气中氧气含量的测定,应在小学自然常识的基础上加深一步。对剩余的气体,应进行检验,使学生对氮气也应有 所了解。在钟罩内演示,剩余气体不好检验;通过水槽,再观察钟罩内的水,上升1/5,不易观察;钟罩内的水位上升,水槽内的水位下降,势必造成一个水位差,使钟罩内的水不易上升到1/5,又不太科学。为此,改进如下: 1、实验方法
(1)首先找一段粗玻璃管,直径约2-3cm,长约20-25cm,或用破底的大号试管代替。下口配带导管的单孔胶塞,上口配带活门的单孔胶塞,并在胶塞中插入两根粗一些的铜丝,将胶塞小头一边的铜丝砸扁,弯成钩状。取300-500瓦的电炉丝一小段(约8-10个自然圈),两头用钳子加直,放在铜丝钩上,并用钳子夹紧。外边的两根粗铜丝,与6伏电源连接,作为量气管。
再找一个塑料瓶(如矿泉水瓶),将底去掉,小口配带导管的单孔胶塞,用胶管与量气管连接,固定在铁架台上,如图6-1所示。
图6-1
(2) 在水中滴几滴红墨水,将量气管上的活门打开,从塑料瓶中注水,约到量气管容积的1/4后止。从量气管口上套入四根红色皮筋,用皮筋将量气管中的空气五等分。
(3)将带电池组的胶塞拔出,切一小条白磷插入电炉丝中,再将胶塞重新塞入量气管口,并塞紧。 (4)接通电源,让学生观察所发生的两种现象,量气管中产生大量白烟,为什么,量气管中的红色水面下降,为什么,待反应停止后将电源切断,再让学生观察,红色水面又逐渐上升,为什么,当红色的水面上升至快接近红色标线时,即不在上升追问学生为什么,并再让学生观察塑料瓶与量气管中的红色水面是否在同一个水平面上,若不在同一个水平面上,又会产生会什么现象,
(5)从塑料瓶口慢慢注入水,使两个液面达到同一水平,这时学生即可发现,量气管中的水面又稍有上升,正好达到标线。根据上述实验现象,引导学生分析,得出空气中氧气的含量,按体积计算,约占空气体积的1/5的结论。 再追问学生,量气管中剩余的又是什么气体,并引导学生回忆小学学过二氧化碳气体的性质:第一它能灭火,第二能使澄清的石灰水变浑浊。再引导学生看看剩余的又是什么气体,
(6)在塑料瓶中再注入一些水,将小木条点燃,放在带活门的玻璃尖嘴处,将活门打开,学生马上会发现火苗熄灭,他们立刻就会回答,是“二氧化碳”,这时教师不要忙于马上纠正学生的答案,请学生继续观察下边的实验。 (7)取一支试管,注入少量澄清石灰水,在玻璃尖嘴处,接上玻璃导管,并将玻璃管插入试管中。在塑料瓶中,再注入一些水,打开活门,再让学生观察现象,他们又会发现,试管中只冒气泡,石灰水并不浑浊。根据现象,追问学生,剩余的气体是不是二氧化碳,分析后,教师引导学生得出结论,剩余气体绝大部分是氮气,它与二氧化碳一样能灭火,但又与二氧化碳不同,不能使澄清的石灰水变浑,这就是氮气的部分性质。
2、实验说明
(1)由于白磷易燃,实验时与实验后,要妥善处理。
(2)量气管中的水,不能注入太少。若水注入太少,白磷在反应时,由于气体受热膨胀,会将全部水压入塑料瓶中,从而量气管中的部分气体,就会从塑料瓶中溢出,造成实验失败。水的量最少应占量气管体积的1/4。 (3)氧气按体积计算,大约占空气的1/5。但氧气与白磷反应,氧气不能全部参加反应,当氧气的浓度逐渐变小时,达到一定的限度,就再不能与白磷反应,要想准确地测得达到1/5是不太容易的。
范文五:空气成分探究实验的变形练习
关于“空气成分探究?实验”的变形练习 教材中的实验?“空气中氧气含?量的测定”是中考命题的?热点问题。考题多以空气?成分的测
定原?理、装置、现象及误差分?析等为切入点?。现将此类考题?的相关变形介?绍给大家,希望
能对同学?们学习过程中?辩证思维的培?养起到抛砖引?玉的作用。
例1:把足量的红磷?和硫粉分别放?在等体
积的A?、B两个盛满空?气的集气瓶(气密性良
好)中燃烧。如图所示,烧杯中盛放的?是
水,燃烧前夹紧止?水夹。燃烧完毕冷却?后,
打开止水夹,烧杯中的水会?很快进入 瓶,此现象产生的?原因是 ,进入水的体
积?约 (填“等于”、“大于”或“小
于”)集气瓶容积的?是 。
例2:把足量的红磷?和硫粉分别放?在
等体积的A?、B两个盛满空?气的集气瓶(气
密性良好)中燃烧。如图所示,烧杯中盛
放的?是水,燃烧前夹紧止?水夹。燃烧完
毕冷却?后,打开止水夹,烧杯中的水会?
进入 瓶,此现象产生的?原因
是 。进入瓶中水的?体积会 (填
“大于”、“小于”或“等于”)集气瓶
容积的? 。
例3:小明同学为证?实空气中氧气?的体积分数,进行如图所示?的实验。燃烧匙里盛放?足量的硫粉,反应结束,冷却后打开止?水夹,水沿导管进入?A瓶。请回答:(1)、B容器的名称?是 。
(2)、该实验失败的?主要原因: 。
(3)、若不改变原装?置,要使实验成功?,你的改进意见?是: 。
(4)、若实验成功,A瓶里的水大?约可以达到A?瓶容积的 。由此证明空气?中氧气的
体积?分数约为: 。
例4:某研究性学习?小组设计如图?所示的设置,探究空气2中氧?气的体积分数?,其中A是底面?积为50cm,?高20cm的?圆柱形玻璃容?器(带密封盖)上面标以cm?为单位的刻度?,B是带刻度的?敞口玻璃管(其他辅助装置?略),他们的操作过?程如下:a、检查装置气密?性;b、加入水并调整?B的高度,
使A的液面至?刻度15cm?处;c、将过量的铜粉?平
铺在惰性电热?板上,盖紧封盖;d、通电加热铜粉?,
待充分反应后?,冷却到原来的?状况,调整B的高度?, 使容器A、B中液面保持?水平。记录液面的刻?度。
(注:A容器内固态?物质所占的体?积忽略不计)
(1)、在操作a中,检查装置气密?性的方法是: 。 (2)、在上述实验中?,下列物质不能?代替铜粉的是?:( )。 A、红磷 B、碳粉 C、铁粉
(3)、在操作d结束?时,装置A中液面?的刻度约为 cm,如果在操作d?结束时,装置A中液面?的刻度在11?cm处,则实验结束比?理论值 (大或小)。
(4)、该小组中由同?学提出用木炭?代替铜粉也能?测定空气中氧?气的体积分数?,只要求将水换?成一种溶液,则该溶液具有? 性质,其原因
是: 。
例5:利用图示装置?可以粗略的测?定空气的组成?,玻璃
活塞左端密封?有空气,活塞右管内有一?可左右移动的?活塞。
端的玻?管与大气相通?,烧杯中加入适?量的生石灰,再向烧杯
中加?入水,观察现象并回?答问题:
(1)、玻璃管内白磷?与红磷的组成?相同,所以
白磷的燃烧现?象是 ,反应后文字表?达式
为 。玻璃管冷却后?,活塞会
向 移动,原因是: 。
(2)、实验结束后,恢复到原来温?度,活塞应
停留在约 的刻度处,通过实验得出?的正确结论是? 。 (3)、已知:镁和氧气在点?燃的条件下生?成氧化镁,镁和氮气
在点?燃的条件下生?成氮化镁;想一想能否用?镁来代替白磷?测定
空气空气?中氧气的含量?,为什么,
例6:某同学测定空?气里氧气含量?设计了如图装?置,该同学
在“金属梯”的每一个凹处?放置一颗用滤?纸吸干水后的?白磷,
用放大镜会聚?6V手电筒光?于靠近水面的?一步“金属梯”处的白
磷上,请回答下列问?题。
(1)、一段时间后,可观察到的现?象是: 。
(2)、“金属梯”的每一步上都?放置一小颗
白磷与只靠近?水面的一步“金属梯”处放一大颗白?磷相比,
优点是: 。
例7:二硫化碳是一?种无色液体,易挥发,能溶解白磷、碘
等物质。白磷能自燃生?成五氧化二磷?。现有甲、乙两个集气瓶?均盛有空气,现将浸有一
小?块白磷的二氧?化硫溶液的滤?纸,待二氧化硫挥?发后,立即将滤纸投?入到乙瓶中。装置
完毕后,天平调至平衡?,室温下过一段?时间,天平指针将偏?向,理由: 。 例8:某校研究性学?习小组用右下?图装置进行镁?条在空气中燃?烧的实验,燃烧、冷却后打开
止?水夹,进入集气瓶中?水的体积约占?集气瓶体积的?70%。
(1)右图A仪器的?名称是 ,燃烧、冷却后打开止?水夹,水能进入集气?瓶的原因
是 。
(2)如果镁条只和?空气中的氧气?反应,则进入集气瓶?中水的体积最?多
不超过其容?积的 %。现进入集气瓶?中水的体积约?为其容积的
7?0%,根据空气的组?成可推出减少?的气体中有氮?气。
【发现问题】氮气是怎样减?少的呢,
【假设一】氮气与镁条反?应而减少。
【假设二】 。
【查阅资料】镁条在氮气中?能燃烧,产物为氮化镁?(MgN)固体。氮化镁中氮元?素的化合价为32
? 。镁条还可以在?二氧化碳气体?中燃烧生成碳?和氧化镁,该反应类型是?。 (3)通过以上探究?,你对燃烧的有?关知识有了什?么新的认识: (写出一点即可?)。
转载请注明出处范文大全网 » 演示实验:空气的成分



 是干不是干
是干不是干

