范文一:测定氧气含量实验追踪
测定氧气含量实验追踪
226400 江苏省如东县实验中学 缪徐
空气中氧气含量的测定实验,一直是近几年来各地中考的热点。对于这一热点,我们可以从以下几个方面来加以追踪。
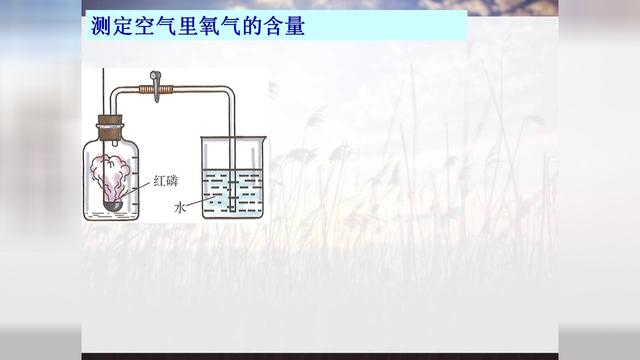
1.原理探询:空气中的氧气与红磷反应生成固态的五氧化二磷,导致盛装空气的容器中气压减小,水被压进装置,根据进入装置中水的体积可测算出空气中氧气的体积分数。该实验运用的是化隐性为显性的设计思想,即将空气中氧气体积分数这一看不见的现象,通过水的“介入”而显现了出来。
2.现象描述:红磷燃烧过程中产生大量的白烟;等红磷熄灭并冷却后,观察到钟罩内水面上升约1/5体积。
3.结论推理:(1)由钟罩内水面上升约1/5体积,可推出空气中氧气的体积约占1/5;(2)由过量的红磷燃烧停止,可推出空气中其它成分(如氮气、稀有气体等)化学性质稳定;(3)由水面上升到一定程度就不再上升,可推出空气中的其它成分不易溶于水。
4.疑难剖析:
(1)导致该实验测定结果偏小的原因可能有哪些,
红磷的量不足,会导致钟罩内的氧气消耗不尽;装置气密性不好,会导致钟罩外的空气进入钟罩内;温度高于室温,会导致钟罩内的气压变大。上述三种情况,都可能引发进入钟罩内的水的体积小于钟罩体积的1/5,从而导致测定结果偏小。因此,在上述测定实验中要注意掌握好三个操作要点:?红磷必须是过量的;?装置的气密性必须良好;?观察钟罩内水面变化的时机是等实验装置冷却以后。
(2)该实验中的红磷能够用木炭代替吗,
木炭也能与空气中的氧气发生反应,生成二氧化碳气体。该反应虽然也能消耗钟罩内的氧气,但由于生成的二氧化碳气体基本上能填补氧气的“体积空缺”,不会导致钟罩内的气压发生明显的改变,实验中也就难以观察到水面上升的现象。因此,该实验中一般不用木炭代替红磷(注:等学习了碱的化学性质后,我们将会知道,对该实验作适当的改进后,也可以用木炭代替红磷测定氧气的含量)。
联系电话:0513—84010990;13823626699;电子信箱:jsrdmx@163.com
范文二:测定氧气含量实验探究
测定空气中氧气含量的探究实验
1、实验药品选择型
小军根据燃烧红磷测定空气中氧气含量的实验原理,认为可用木炭替代红磷测定空气中氧
气的含量,并按左下图所示装置进行实验。
(1)依据的实验原理是_______________________________。
小军检查装置气密性后,将盛有足量红热木炭的燃烧匙迅速伸入广口瓶中,并把塞子塞紧,待红热的木炭熄灭并冷却至室温后,就打开弹簧夹,并未发现倒吸现象。经过认真分析,小军发现实验失败的原因是(答一条)
________________________________________________。
(2)小军反思上述实验的探究过程后认为:用燃烧法测定空气中氧气含量的实验时,在药品的选择和生成物的要求上应考虑是(答一条)
__________________________________________________________。
2、实验误差分析型
某班同学用右图装置测定空气里氧气的含量。先用弹簧夹夹住乳胶管。点燃红磷伸 入瓶
中并塞上瓶塞。待红磷熄灭并冷却后,打开弹簧夹,观察 广口瓶内水面变化情况。
实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的1/5,乙同学的广口瓶
内水面上升显大于瓶内空气体积的1/5。下列对这两种现象解释合理的是( )
?甲同学可能使用的红磷量不足,瓶内氧气没有消耗完
?甲同学可能未塞紧瓶塞,红磷熄灭冷却时外界空气进入瓶内
?乙同学可能没夹紧弹簧夹,红磷燃烧时瓶内空气受热从导管逸出
?乙同学可能插入燃烧匙太慢,塞紧瓶塞之前,瓶内空气受热逸出
A.只有?? B.只有?? C.只有??? D.???? 归纳:实验结果比实际偏低,原因可能有
实验结果比实际偏高,原因可能有
三、实验装置创新型
1、 为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为40 mL的试管
作反应容器,将过量的白磷放入试管,用橡皮塞塞紧试管口,通过导管与实际容积为
60 mL且润滑性很好的针筒注射器组成如右图的实
验装置。 假设此实验能按照小华的设想正常进
行,且白磷所占体积与导管内的气体体积忽略不
计,请回答下列问题:
(1)实验前,打开弹簧夹,将注射器的活塞前沿从20 mL刻度处推至15mL刻度处,然后
松手,若活塞仍能返回至20mL刻度处,则说明____________________。
(2)若先夹紧弹簧夹,用酒精灯加热白磷,燃烧结束,等到试管冷却后再松开弹簧夹。
可观察到的现象为_______________________________________________。
3)若不使用弹簧夹,用酒精灯加热白磷,充分反应直至燃烧结束,试管冷却。可观察(
到的现象为______________________________________________________________。
(4)若按小华的设想进行实验,实际可能遇到诸多问题而发生危险,造成实验失败。例
如______________________________________________________________________。
2、某同学为测定空气里氧气的含量,设计了如图3所示的实验装置。该同学在
“金属梯”的每一步的凹处放置一颗用滤纸吸干水后的白磷,
用放大镜会聚6V手电筒光于靠近水面的一步“金属梯”处的
白磷上。请回答问题:(1)一段时间后,可观察到的现象是 。
(2)“金属梯”的每一步上都放置一小颗白磷与只靠近水面的一步“金属梯”处放一大颗
白磷相比,优点是 。
白磷白磷
金属梯金属梯
太阳光 太阳光 红磷 水 水 白???????? ???????? 磷
范文三:氧气含量测定探究实验
第二单元 课题1 空气(一) 学案
一、用2分钟阅读课本P 26“空气是由什么组成的”。
讨论交流:
1)空气是一种单一的物质吗?
2)拉瓦锡研究空气成分的实验中,当密闭容器中将汞连续加热12天后,
发生了什么现象?
3)实验中提到:容器内空气的体积大约减少了1/5,又是通过什么现象得
知的呢?
4)拉瓦锡加热至12天时,发生的反应用文字表达式表示为:
反应方程式为:
将上述实验得到的红色粉末再放入密闭容器中加强热,即可得到汞(Hg)和
氧气(O 2)。请写出此反应的文字表达式:______________________________。
反应的方程式为:
5) 拉瓦锡所做实验的最终结论是__________________________________。
二、【实验探究】:空气中氧气体积含量的测定
1、 实验现象:(注意对红磷在燃烧前、中、后的现象进行仔细观察和描述)
①燃烧前:
②燃烧时:
③熄灭后,冷却打开弹簧夹:
2、思考:
(1)红磷在集气瓶中燃烧,消耗了什么气体?
(2)红磷在集气瓶中未能全部燃烧,说明了什么?
(3)在这个实验中燃烧的物质为什么会选用红磷?
(4)集气瓶中剩余的气体主要是什么?有什么性质?
(5)打开止水夹后,为什么集气瓶中能吸入水?
(6)集气瓶底部放一些水的原因是:
3、该反应的文字表达式为:
该反应的化学方程式为:
4、讨论交流:
⑴可能导致进入瓶内水的体积明显小于瓶体积的1/5的原因有哪些?
⑵可能导致进入瓶内水的体积明显大于瓶体积的1/5的原因有
(3)用木炭或硫粉来代替红磷可以吗?为什么?如果实验没有红磷了,改用硫粉或木炭来代替,可以怎样改进装置来达到目的?
5、实验结论:
6、认识相似的装置:
思考:改进装置与课本中的装置比较各有哪些优缺点?
范文四:氧气含量测定实验汇总
空气中氧气含量测定实验的拓展
1.将足量的下列物质分别放在燃烧匙上点燃(或灼烧),分别放入四只下图所示装置的广口瓶中,立即塞紧橡皮塞,反应结束待冷却后,打开止水夹,导管中水柱上升最少的是放入哪种物质的装置,( ) A.铁粉 B.磷 C.木炭 D.镁
2.某班同学用下图装置测定空气里氧气的含量。先用弹簧夹夹住乳胶管。点燃红磷,伸入瓶中并塞上瓶塞。待红磷熄灭并冷却后,打开弹簧夹,观察广口瓶内水面变化情况。实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的1/5,乙同学的广口瓶内水面上升明显大于瓶内空气体积的
1/5。下列对这两种现象解释合理的是( )
?甲同学可能使用红磷的量不足,瓶内氧气没有消耗完
?甲同学可能未塞紧瓶塞,红磷熄灭冷却时外界空气进入瓶内
?乙同学可能没夹紧弹簧夹,红磷燃烧时瓶内部分空气受热从导管逸出
?乙同学可能插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出
A.只有?? B.只有?? C.只有??? D.只有????
3.上图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。下列说法中不正确的是( )
A(该实验证明空气中氧气的含量约占1/5 B(实验时红磷一定要过量
C(实验前一定要检验装置的气密性 D(红磷燃烧产生大量的白雾,火焰熄灭后立刻打开弹簧夹 4(根据空气的成分填空,小兰同学用上图装置进行实验,结果发现测得的氧气体积分数大于1,5,请你帮助她分析造成这种结果的可能原因是: 5(空气、水是人类赖以生存的自然资源。
(1)测定空气中氧气体积分数的实验装置如右图所示。在集气瓶内加入少量的水,并五等分水面以上的容积,做上记号。用弹簧夹夹紧乳胶管。点燃燃烧匙内足量的红磷后,立即伸入瓶中并把塞子塞紧。
?写出红磷在空气中燃烧的化学方程式: 。
?待红磷熄灭并冷却后,打开弹簧夹,观察到烧杯中的水进入集气瓶,瓶内水面最终上升约至1刻度处。由此可知氧气约占空气总体积的 。
?红磷熄灭后,集气瓶内剩下的气体主要是 ,该气体 (填“支持”或“不支持”)燃烧。
6. 右图所示装置也可用来测定空气中氧气的含量。该实验认识正确的是( )
A(选用红磷是因为反应可以耗尽O,生成固态的PO 225
B(燃烧匙中的红磷可以换成硫或木炭
C(燃烧匙中的红磷越多,水位上升越高
D(本实验可以证明空气含有,、O、CO和稀有气体 222
7.为测定空气中氧气所占的体积分数,某同学设计了右图所示的实验,在一个耐热活塞的底部放一小块(足量)白磷(白磷在空气中燃烧的温度为40 ?),然后迅速将活塞下压,可以观察到的现象为 ;冷却至原来温度时,松开手,活塞最终将回到刻度 处,试回答白磷燃烧的原因 。
8.研究性学习小组的同学为探究空气中氧气的体积分数,设计了右图所示装置。
请根据图示实验回答下列问题:
(1)闭合电源开关,可以观察到白磷___________。
(2)装置冷却到室温,可观察到U型管内左侧液面_________。
(3)通过这个实验得出的结论是______________。
(4)此实验还可推知反应后剩余气体的两点性质是:__________;______________。
9.某校化学兴趣小组就空气中氧气的含量进行实验探究:[集体讨论]:
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体。他们应该选择( ) A(蜡烛 B(红磷 C(硫粉
为了充分消耗容器中的氧气,药品的用量应保证 。
(2)小组同学共同设计了如图4的两套装置, 你认为合理的是(填编
号) 。为了确保实验的成功,在装药品之前应
该 。
[分组实验] 在讨论的基础上,他们分组进行了实验。
[数据分析] 实验结束后,整理数据如下:(注:集气瓶容积为100 mL)
组 别 1 2 3 4 5 6
进入集气瓶中水的体积(mL) 20 21 19 20 22 1
8 (3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的 。 通过实验还可以推断集气瓶中剩余气体的性质是 。 (4)小组的同学做完实验后又尝试用木炭重新做了以上实验,发现水几乎没有进入集气瓶。经讨论,同学们一致认为如果事先在集气瓶内注入少量 溶液来吸收 气体,实验也能取得较好的效果。
(5)某同学对实验进行反思后,提出了改进方法(图5所示 ),你认为改进后的优点是:
10.某同学用右图所示的装置粗略地测定空气中氧气的体积分数,图中烧杯上方玻璃管(预先固定好)中部有一可左右滑动的活塞,活塞左端管内密封有空气,活塞右
端的玻璃管口跟空气连通,实验开始前活塞处在刻度5 cm处。已知生石灰与水反
应能产生大量的热;可燃物燃烧必须同时具备二个条件,一是有一定的温度;二
是有充足的氧气。
?向烧杯内加入适量水,与生石灰反应的目的是 。
?可观察到玻璃管内开始发生的现象:白磷(足量) ,活塞向 (填“左”或“右”)移动。
?实验结束,恢复到常温后,活塞应停在约 cm处,据此可得出的结论是:
。
11.为粗略测量空气中O与N的体积比,某学生设计了右图所示的实验装置进行实验。实验时,先关闭弹22
簧夹a,将螺旋状的铜丝在酒精灯的灼烧后迅速插入大试管,接触试管底部的过量的白磷,然后立即塞紧橡皮塞。由于白磷的着火点比红磷低得多,因此反应很容易发生,可观察到大试管中产生大量的白烟。试回答以下问题:
(1)试写出白磷燃烧的符号表达式
(2)待试管冷却后打开弹簧夹,此时可观察到的现象为 , 据此可证实空气中O与N的体积比大约为 。 22
(3)如果装置气密性不好,则测出的O与N的体积比将 。(填“偏22
大”、“偏小”、或“不变”)。
12.某同学为测定空气里氧气的含量,设计了如图3 所示的实验装置。该同学在“金属梯”的每一步的凹处放置一颗用滤纸吸干水后的白磷,用放大镜会聚6V手电筒光于靠近水面的一步“金属梯”处的白磷上。
回答下列问题:
?一段时间后,可观察到的现象是_________________。
?“金属梯”的每一步上都放置一小颗白磷与只靠近水面的一步“金属梯”处放一大颗白磷相比,优点是______________________。
13(甲生按右图组装仪器,关闭止水夹,通电使红磷燃烧。请回答下列问题:
(1)燃烧的现象是 ;
(2)红磷燃烧一段时间后,自动熄灭了,你认为原因
是 ;
(3)冷却后,松开止水夹,你观察到的现象为 。 (4)乙生用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏差,其操作上的原因可能是(要求答出两种):
, 。 (5)丙生也设计了一个实验方案,装置和操作同上,只不过用木炭代替了红磷。当木炭停止燃烧,集气瓶冷却至室温,打开铁夹后,水能否进入集气瓶,为什么,
。 (6)若仍然用木炭代替红磷,丙生的实验方案应作何改进,才能保证实验成功,(只需答出实验方案中须改进的地方)
。 (用下图14所示装置测定空气中氧气的含量。 14
(1)实验时,取下橡胶塞,点燃红磷迅速伸入集气瓶中并塞紧橡胶塞,这时看到的现象是__________________________________________。
(2)小倩设计了如下图15所示的改进装置,其优点是不污染空气或操作简便或实验误差较小(只写一点)。从理论上分析,玻璃管内液面最终将上升至___处(填1、2、3、4),但实验测结果液面往往偏低,其原因可能是____________________________________________(其他合理答案均可)。(只写一条)
14 图 15 图
15(某科学兴趣小组查阅资料得知镁可在氮气中燃烧生成MgN,设计了如下方案进行验证。 32
步骤1:用盛水的水槽、无底的废广口瓶、燃烧匙、蒸发皿、橡皮塞等装配成如右上图所示的装置。另准备一只有一根铜丝穿过的橡皮塞,铜丝末端固定一根镁条。
步骤2:引燃燃烧匙中足量的红磷,塞好橡皮塞。待充分冷却,观察到广口瓶内水面上升的体积约占瓶内水面原上方空间的1,5左右。
步骤3:往水槽中加水使广口瓶内外水面相平。点燃镁条,更换橡皮塞,镁条在广口瓶内继续燃烧,发出红光,放出热量。待冷却后广口瓶内水位继续上升。
(1)步骤2的目的是 。
(2)在步骤3“待冷却后广口瓶内水位继续上升”是由于瓶内气压 (选填“大于”“小于”或“等于”)外界气压。
(3)根据上述实验和你所学的知识,请写出镁在空气中燃烧时的化学方程式:
16(某课外活动小组在学习了书本 “空气中氧气含量的测定”实验,知道PO不能随便排放在空气中,否25
则会对空气造成污染,所以对该实验进行了改进:
在由两个注射器组成的密闭系统内共有50 mL空气,如右图。然后给装有红磷的玻璃管加热。同时交替推动两个注射器的活塞,至玻璃管内的红磷变成白烟,且较长时间内无进一步变化时停止。停止加热后,待冷却至室温将气体全部推至一个注射器内。
请根据你对上述实验的理解,回答下列问题:
(1)实验结束后,注射器内的气体体积理论上应该减少
约 mL。
(2)在实验的加热过程中,交替缓慢推动两个注射器的目的
是 。写出该反应的化学方程式
(3)上述实验只是粗略测定空气中氧气含量的一种方法,你认为造成该实验不够精确的可能原因是 (写出其中一种) 。
17(某化学兴趣小组对教材中“测定空气
里氧气含量”的实验(见图11)进行了大
胆改进,设计图12)(选用容积为45mL
的18×180mm的试管作反应容器)实验方
案进行,收到了良好的效果。请你对比分
析下面图11、图12实验,回答下列有关问题: (1)指出实验中A、B仪器的名称:A______________、B________________。
(2)图11实验中发生反应的化学方程式为__________________________________________________。 (3)图12实验的操作步骤如下:?点燃酒精灯。?撤去酒精灯,待试管冷却后松开弹簧夹。?将少量红磷平装入试管中,将20mL的注射器活塞置于10mL刻度处,并按图12中所示的连接方式固定好,再将弹簧夹紧橡皮管。?读取注射器活塞的数据。
你认为正确的实验操作顺序是__________________________________________________(填序号)。 (4)图12实验中,注射器活塞将从10mL刻度处慢慢前移到约为__________________ mL刻度处才停止。 (5)对照图12实验,你认为图11实验有何不足之处,(回答一点即可)
__________________________________________________ 。
18(为测定空气中氧气的含量,小华同学打算设计如下方案:选用实际容积为40 mL的试管作反应容器,
将过量的白磷放入试管,用橡皮塞塞紧试管口,通过导管与实
际容积为60 mL且润滑性很好的针筒注射器组成如右图的实验
装置。假设此实验能按照小华的设想正常进行,且白磷所占体
积与导管内的气体体积忽略不计,请回答下列问题:
(1)实验前,打开弹簧夹,将注射器的活塞前沿从20 mL刻度处推至15mL刻度处,然后松手,若活塞仍能返回至20mL刻度处,则说明____________________. (2)若先夹紧弹簧夹,用酒精灯加热白磷,燃烧结束,等到试管冷却后再松开弹簧夹。 可观察到的现象为_______________________________________________。
(3)若不使用弹簧夹,用酒精灯加热白磷,充分反应直至燃烧结束,试管冷却。可观察到的现象为___________________________________________________ (4)若按小华的设想进行实验,实际可能遇到诸多问题而发生危险,造成实验失败。例如___________________________________________________
范文五:关于“空气中氧气含量的测定”实验误差分析的实验报告[权威资料]
关于“空气中氧气含量的测定”实验误差分析的实验报告
本文档格式为WORD,若不是word文档,则说明不是原文档。
最新最全的 学术论文 期刊文献 年终总结 年终报告 工作总结 个人总结 述职报告 实习报告 单位总结
【内容摘要】在课堂的演示实验中,学生对“空气中氧气含量的测定”实验的误差分析提出了质疑,因此本文针对学生的质疑进行了探究,得出了相关结论,即未冷却就打开止水夹,在本实验的条件下,进水体积偏小。
【关键词】氧气含量 误差分析 进水体积
科粤版九年级化学教材第二章第一节“空气的成分”中,选取了利用红磷在空气中燃烧的实验来测定空气中氧气的含量。
对于此实验的误差分析中有一条认为:若广口瓶未冷却至室温就打开止水夹,则会造成测定结果偏小。
在课堂探究中,有学生提出,若未冷却就打开止水夹,可能还有其他两种情况出现:第一种,瓶内气压可能大于导管末端压强,气体从导管末端逸出,逐渐冷却到室温后,最终进入广口瓶中的水的体积大于1/5;第二种,瓶内气压可能小于导管末端压强,水进入广口瓶后,一方面水会使气体冷却,另一方面也在与外界进行热交换而冷却,故若时间足够,最终进入瓶中的水的体积应约等于1/5。
结合学生的看法,我们与学生共同设计方案进行探究。
1实验目的
探究未冷却至室温就打开止水夹,进水体积与正常值的比较。
2实验原理
红磷在密闭容器内的空气中燃烧,消耗氧气,生成P2O5固体,使瓶内压强减小,小于外界压强,产生压强差。
打开止水夹,水就会流入密闭容器内。流入密闭容器内的水的体积即为消耗的氧气的体积,由此测定空气中氧气的含量。
如果红磷的量充足,瓶内氧气会被全部消耗,因为氧气的体积在空气中所占比例约为1/5,因此进水量也应约为广口瓶内气体体积的1/5。
反应方程式:
3实验药品及仪器
红磷、药匙、广口瓶、燃烧匙、带孔橡胶塞、玻璃导管、橡胶管、止水夹、烧杯、秒表、量筒(50mL、1000mL)、胶头滴管、记号笔。
4实验方法
(1)实验装置
(测定空气中氧气含量实验装置图)
(2)实验步骤
?给广口中瓶装满水,再量出广口瓶中水的体积,即为广口瓶的容积。
?严格按照正确的操作步骤,让瓶中气体冷却至室温(20分钟),打开止水夹,记录最终进水体积;
?红磷刚熄灭时就打开止水夹,冷却至室温(20分钟),记录最终进水体积;
?红磷熄灭1分钟后打开止水夹,冷却至室温(20分钟),记录最终进水体积;
?红磷熄灭3分钟后打开止水夹,冷却至室温(20分钟),记录最终进水体积;
?红磷熄灭4分钟后打开止水夹,冷却至室温(20分钟),记录最终进水体积。
注:每次实验前,给广口瓶中预先加入10mL水。
5实验现象及数据记录
(1)实验时间:2011-9-6,实时气温:22摄氏度。
广口瓶容积:320mL。理论进水量为67.2mL,加上预先加入的10mL水,则最终进水体积的理论值为77.2mL。
(2)实验时间:2011-9-13,实时气温:17摄氏度。
广口瓶容积:320mL。理论进水量为67.2mL,加上预先加入的10mL水,则最终进水体积的理论值为77.2mL。
(3)实验时间:2011-10-13,实时温度:18摄氏度。
广口瓶容积:310mL。理论进水量为65.1mL,加上预先加入的10mL水,则最终进水体积的理论值为75.1mL。
6实验数据分析
第一次实验和第二次实验时,经测定广口瓶容积约为320mL,因为氧气在空气中所占比例为21%,所以理论进水体积应为67.2mL。第三次实验时由于换了新的橡胶塞,经测定广口瓶容积约为310mL,因为氧气在空气中所占比例为21%,所以理论进水体积应为65.1mL。
但由于本实验中空气体积受实时温度的影响较大,再加上系统误差和认为操作的误差,因此会使实际值与理论值有偏差;而且温度也会影响瓶内气体冷却至室温所需的时间。
(1)对第一种假设的讨论:
三次实验均未出现“瓶内气压大于导管末端压强,气体从导管末端溢出”的现象,所以,学生的第一种假设不成立。
(2)对第二种假设的讨论:
第一次实验时,气温为22?,冷却至室温后瓶中进水量为68mL,比理论值77.2mL小,可能是由于气温、系统误差和人为操作误差所致。之后按照实验操作探究,20min后的进水体积均小于68mL,所以学生的假设在本次实验中未能成立;
第二次实验时,气温为17?,冷却至室温后瓶中进水量为74mL,比理论值77.2mL小,可能是由于气温、系统误差和人为操作误差所致。之后按照实验操作探究,20min后的进水体积均小于74mL,所以学生的假设在本次实验中也未能成立。
第三次实验时,气温为18?,冷却至室温后瓶中进水量为71mL,比理论值75.1mL小,可能是由于气温、系统误差
和人为操作误差所致。之后按照实验操作探究,20min后的进水体积均小于71mL,所以学生的假设在本次实验中也未能成立。
结论:在现有实验条件下,学生所假设的两种可能性均不成立。因此,未冷却就打开止水夹会导致测定结果偏小。
7实验误差分析
本次实验由于实验条件的限制,没有精密的仪器进行测定,所以存在一定的系统误差,气温的变化对气体体积的影响和人为操作的不当也会造成误差。
8反思
老师可以在课后和学生对此实验结果再进行分析和讨论,也可让学生组成兴趣小组,利用课余时间查阅相关资料,继续做实验进行探究。
新课标下的化学学习更加注重学生思维和创新能力的培养,特别是化学实验,更加是培养学生创新意识和探究意识的最佳方法。通过本次探究,我们应该更加重视在课堂上激发学生的探究意识,发散学生的思维,鼓励学生提出自己的想法,让学生在学会探究的同时也为我们教师注入新的思维方式。
阅读相关报告总结文档:电子白板让数学课堂更精彩 数学教学中“学案导学法”有效应用之我见 高中数学教学模式研究 初中一次函数图象与性质的探究教学 中学数学教科书中的开放题 探究初中物理教学中学生能力的培养 初中数学“先学后教”课堂教学改革探析 校园垃圾变废为宝 浅谈聋校数学课中难点教学的突破 数学教学中的多媒体运用 幼儿数学教学的有效方法和途径 充分利用班会课加强对新生的教育 高中数学教学兴趣培养研究 论小学数学教学充满生活情趣 浅谈如何在小学数学教学中运用成功教育 在科学教学中渗透环保教育 高中物理教学中,如何培养学生独立思考的能力 高中作息技术促进教学现代化 新教改视域下初高中
*本文若侵犯了您的权益,请留言。*
2013年最新【学术论文】【总结报告】 【演讲致辞】【领导讲话】 【心得体会】 【党建材料】 【常用范文】【分析报告】 【应用文档】 免费阅读下载
转载请注明出处范文大全网 » 测定氧气含量实验追踪



 祈祷23400441
祈祷23400441

