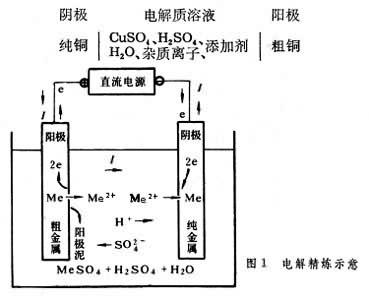
范文一:电解池电极反应式
电解池电极反应式练习
班级 姓名 常见电解池电极反应归纳
(一)、用惰性电极电解电解质溶液
1、 CuCl2溶液
阴极: 阳极: 总方程式:
2、 HCl溶液:
阴极: 阳极: 总方程式: 3、H2SO4溶液:
阴极: 阳极: 总方程式: 4、NaOH溶液:
阴极: 阳极: 总方程式:
5、Na2SO4溶液:
阴极: 阳极: 总方程式:
6、NaCl溶液(氯碱工业)
阴极: 阳极: 总方程式: 7、CuSO4溶液
阴极: 阳极: 总方程式:
8、电解AgNO3溶液
阳极: 阴极: 总方程式:
(二)、用活性电极材料电解电解质溶液
1、铜的电解精炼:粗铜作极,接电源极;精铜作为CuSO4溶液作为电解质溶液。
阳极反应: 阴极反应:
2、电镀:镀层金属做极,镀件做极,含有镀层金属阳离子的盐溶液作为电镀液。
在铁钉上镀铜:铜做 极,接电源 极;铁钉做 极,接电源 极;电镀液采用含 的盐溶液。
阳极反应:;。
(三)、用惰性电极电解下列熔融电解质
1、熔融NaCl
阴极: 阳极: 总方程式: 2、熔融MgCl2
阴极: 阳极: 总方程式: 3、熔融Al2O3(冶炼金属铝)
阴极: 阳极: 总方程式: (四)、根据图示装置写出各电极反应式
1、B、C为铜,A、D为碳
A ____________________________________
B _____________________________________
C _____________________________________
D _____________________________________
2、NaCl溶液中滴酚酞,电极1附近变红
1 ___________________________________
2 ___________________________________
3 ___________________________________
4 ___________________________________
5 ___________________________________
6 ___________________________________
常见电解池电极反应归纳
(一)、用惰性电极电解电解质溶液
1、电解CuCl2溶液
电解
阳极:2Cl—2e==Cl2阴极:Cu+2e==Cu 总:CuCl2 === Cu+Cl2——2+—
2电解HCl溶液 电解
阳极:2Cl—2e==Cl2 阴极:2H+2e==H2总:2HCl === H2+Cl2 ——+—
3、电解H2SO4溶液
电解 阳极:4OH—4 e==2H2O+O2阴极:4H+4e==2H2总:2H2+ O2——+—
4、电解NaOH溶液
电解 阳极:4OH—4 e==2H2O+O2阴极:4H+4e==2H2 总:2H2O === 2H2 + O——+—
5、电解Na2SO4溶液
电解
阳极:4OH—4 e==2H2O+O2阴极:4H+4e==2H2总:2H2O === 2H2+ O2——+—
6、电解NaCl溶液 阳极:2Cl——2e—==Cl2 阴极:2H++2e— ==H2电解 总: 2NaCl+2H2O === H2+Cl2+2NaOH
7、电解CuSO4溶液 阳极:4OH——4 e—==2H2O+O2阴极:2Cu2++4e—==2Cu
电解 总: 2 CuSO4+2H2O === 2Cu+O2+2H2SO4
8、电解AgNO3溶液 阳极:4OH——4 e—==2H2O+O2阴极:4Ag++4e—==4Ag
电解 总: 4 AgNO3+2H2O === 4Ag+O2 +4HNO3
(二)、电解原理应用
1、铜的电解精炼:粗铜作阳极 ,接电源正极;精铜作为阴极,接电源负极 ;硫酸酸化的CuSO4溶液作为电解质溶液。阳极反应:Cu -2e— 2 阴极反应: 2+2e— ++
2、电镀:
2的盐溶液。阳极反+
应:Cu -2e— 2;阴极反应:Cu2+2e— (在镀件上析出)。 ++
范文二:电解池电极反应式书写
电解池电极反应式的书写
一.请写出下列几组常见的电解池的相关原理(以下电极材料均是石墨)
(1)离子定向移动: →阳极; →阴极。
电极反应——阳极: ;阴极: 。
总的方程式: 。
结论:用惰性电极电解不活泼金属的无氧酸盐(除氟化物),实际是电解溶质本身。电解的结果使c(Cu2+)
减小,溶液的pH略有增大。因为Cu2+ +2H2O
(2)离子定向移动: →阳极;
→阴极;
电极反应——阳极:
;阴极: ;
总的方程式: 。
结论:用惰性电极电解无氧酸(除HF),溶质消耗。电解的结果消耗了HCl,即c(H+,
溶液的pH 。
(3)离子定向移动: →阳极; →阴极
电极反应——阳极: ;阴极: ;
总的方程式: 。
结论:用惰性电极电解活泼金属的无氧酸盐,溶质、水同时消耗。电解的结果生成碱,
电解后溶液的pH 。
(4)离子定向移动: →阳极; →阴极
电极反应——阳极: ;阴极: ;
总的方程式: 。
结论:用惰性电极电解不活泼金属的含氧酸盐,溶质、水同时消耗。电解的结果生成酸,
电解后溶液的pH 。
(5)离子定向移动: →阳极; →阴极
电极反应——阳极: ;阴极: ;
总的方程式: 。
结论:用惰性电极电解活泼金属的含氧酸盐实质是电解水。电解后溶液的pH ,等于 。
(6)离子定向移动: →阳极; →阴极
电极反应——阳极: ;阴极: 总的方程式: 。 H2SO4 Na2SO4 CuSO4 NaCl HCl Cu(OH)2 + 2H+
CuCl2 结论:用惰性电极电解含氧酸实质是电解水.电解后,+
(7)离子定向移动: →阳极; →电极反应:阳极: 总的方程式: 结论:用惰性电极电解强碱实质是电解水。电解后,碱的浓度 ,c(OH,
故溶液的pH 。
1 -
二、电解原理的应用
1.电解饱和食盐水 (1)电极反应
阳极反应式: (________反应); 阴极反应式: (________反应)
电解电解--(2)总反应方程式:2NaCl+2H2O=====2NaOH+H2↑+Cl2↑. 离子方程式:2Cl+2H2O=====2OH+H2↑+Cl2↑
(3)应用:氯碱工业制、。
2.电镀右图为金属表面镀银的工作示意图,据此回答下列问题:
(1)镀件作____极,镀层金属银作____极。
(2)电解质溶液是___________________________________。
(3)电极反应:。
(4)特点:极沉积,电镀液的浓度。
3.电解精炼铜
(1)电极材料:阳极为________;阴极为________。 (2)电解质溶液:含Cu2的盐溶液。 +
(3)电极反应:阳极:____________________________;阴极:_____________________________。
4.电冶金:利用电解熔融盐的方法来冶炼活泼金属Na、Ca、Mg、Al等。
电解(1)冶炼钠 2NaCl(熔融)=====2Na+Cl2↑
电极反应:阳极: ,阴极:______________________________。
电解(2)冶炼铝 2Al2O3(熔融)=====4Al+3O2↑
电极反应:阳极: ,阴极: 。
三.右图为以惰性电极进行电解:
(1)写出A、B、C、D各电极上的电极方程式:
; 。
。
(2)在A、B、C、D各电极上析出生成物的物质的量比为。
四.对于下列装置中的反应,写出相应的电极反应式:
(1)甲装置中,Zn极: Ag。
(2)乙装置中,Cu极:; Ag 。
(3)丙装置中,Fe极: C。
(4)丁装置中,Pt极:Fe。
2
电解池电极反应式书写 答案
电解-+--一.(1)Cl;Cu2;2C1――2e=C12↑;Cu2++2e=Cu; Cu2++2C1―=====C12↑+Cu。
电解-+--+-(2)Cl;H;2Cl-2e===Cl2↑;2H+2e===H2↑; 2H++2C1―=====C12↑+H2↑。
减小;增大。
(3)Cl;Na;2Cl-2e===Cl2↑;2H2O+2e===H2↑+2OH;
电解-2H2O+2C1―=====C12↑+H2↑+2OH。增大。
(4)SO42;Cu2;2 H2O-4e===O2↑+4H;Cu2++2e=Cu; -+-+--+----
电解+2H2O+2Cu2+===== 2Cu+O2↑+4H。减小。
(5)SO42;Na; 2 H2O-4e===O2↑+4H; 2H2O+2e===H2↑+2OH; -+-+--
电解2H2O===== 2H2↑+O2↑。不变;7。
电解-+-++-(6)SO42;H;2H2O-4e===O2↑+4H;2H+2e===H2↑;2H2O===== 2H2↑+O2↑。
增大;增大;减小。
(7)OH;Na;4OH-4e=O2↑+2H2O;2H2O+2e===H2↑+2OH;
电解 2H2O===== 2H2↑+O2↑。增大;增大;增大。
二.(1)2Cl-2e===Cl2↑;氧化。2H+2e===H2↑;还原。 (3)烧碱、氯气、氢气
2.(1)阴、阳; (2)AgNO3溶液等含镀层金属阳离子的盐溶液
(3)Ag-e===Ag;Ag+e===Ag (4)阳、阴、不变
3.(1)粗铜 纯铜 (3)Cu-2e===Cu2;Cu2+2e===Cu -++--++---+--+----
4.(1)2Cl-2e===Cl2↑; 2Na+2e===2Na
(2)6O2-12e===3O2↑; 4Al3+12e===4Al --+---+-
三. (1)Cu2++2e=Cu; 2C1――2e=C12 ;4OH-4e=2H2O+O2↑; 2Ag++2e=2Ag -----
(2)2∶2∶4∶1
四.(1)Zn-2e=Zn2 ;2H+2e===H2↑ (2)Ag+e===Ag↓ ;Ag-e===Ag -++-+--+
(3)Fe-2e=Fe2+; 2H+2e===H2↑ (4)2I―2e=I2 ;2H+2e===H2↑ -+-―-+-
3
范文三:电解池电极反应式书写
------------------------------------------------------------------------------------------------
电解池电极反应式书写
电解池电极反应式的书写
一(请写出下列几组常见的电解池的相关原理(以下电极材料均是石墨)
(1)离子定向移动: ?阳极; ?阴极。
电极反应——阳极: ;阴
极: 。
总的方程式: 。
结论:用惰性电极电解不活泼金属的无氧酸盐(除氟化物),实际是电解溶质本身。电解的结果使c(Cu2+)
减小,溶液的pH略有增大。因为Cu2+ +2H2O
(2)离子定向移动: ?阳极;
?阴极;
电极反应——阳极:
;阴极: ;
总的方程式: 。
结论:用惰性电极电解无氧酸(除HF),溶质消耗。电解的结果消耗了HCl,即c(H+,
溶液的pH 。
(3)离子定向移动: ?阳极; ?阴极
电极反应——阳极: ;阴
——————————————————————————————————————
------------------------------------------------------------------------------------------------
极: ;
总的方程式: 。
结论:用惰性电极电解活泼金属的无氧酸盐,溶质、水同时消耗。电解的结果生成碱,
电解后溶液的pH 。
(4)离子定向移动: ?阳极; ?阴极
电极反应——阳极: ;阴
极: ;
总的方程式: 。
结论:用惰性电极电解不活泼金属的含氧酸盐,溶质、水同时消耗。电解的结果生成酸,
电解后溶液的pH 。
(5)离子定向移动: ?阳极; ?阴极
电极反应——阳极: ;阴
极: ;
总的方程式: 。
结论:用惰性电极电解活泼金属的含氧酸盐实质是电解水。电解后溶液的pH ,等于 。
(6)离子定向移动: ?阳极; ?阴极
电极反应——阳极: ;阴极:
总的方程式: 。 H2SO4 Na2SO4 CuSO4 NaCl HCl Cu(OH)2 + 2H+ ——————————————————————————————————————
------------------------------------------------------------------------------------------------
CuCl2 结论:用惰性电极电解含氧酸实质是电解水.电解后,+
(7)离子定向移动: ?阳极; ?电极反应:阳极: 总的方程式:
结论:用惰性电极电解强碱实质是电解水。电解后,碱的浓度 ,c(OH,
故溶液的pH 。
1 ,
二、电解原理的应用
1(电解饱和食盐水 (1)电极反应
阳极反应式: (________反应); 阴极反应式:
(________反应)
电解电解,,(2)总反应方程式:2NaCl,2H2O=====2NaOH,H2?,Cl2?. 离子方程式:2Cl,2H2O=====2OH,H2?,Cl2?
(3)应用:氯碱工业制、。
2(电镀右图为金属表面镀银的工作示意图,据此回答下列问题:
(1)镀件作____极,镀层金属银作____极。
(2)电解质溶液是___________________________________。
(3)电极反应:。
(4)特点:极沉积,电镀液的浓度。
3(电解精炼铜
(1)电极材料:阳极为________;阴极为________。 (2)电解质溶液:含Cu2的盐溶液。 ,
——————————————————————————————————————
------------------------------------------------------------------------------------------------
(3)电极反应:阳极:____________________________;阴极:_____________________________。
4(电冶金:利用电解熔融盐的方法来冶炼活泼金属Na、Ca、Mg、Al等。
电解(1)冶炼钠 2NaCl(熔融)=====2Na,Cl2?
电极反应:阳极: ,阴极:______________________________。
电解(2)冶炼铝 2Al2O3(熔融)=====4Al,3O2?
电极反应:阳极: ,阴极: 。
三(右图为以惰性电极进行电解:
(1)写出A、B、C、D各电极上的电极方程式:
; 。
。
(2)在A、B、C、D各电极上析出生成物的物质的量比为。
四(对于下列装置中的反应,写出相应的电极反应式:
(1)甲装置中,Zn极: Ag。
(2)乙装置中,Cu极:; Ag 。
(3)丙装置中,Fe极: C。
(4)丁装置中,Pt极:Fe。
2
电解,,,,一.(1)Cl;Cu2;2C1――2e,C12?;Cu2++2e,——————————————————————————————————————
------------------------------------------------------------------------------------------------
Cu; Cu2+,2C1―=====C12?,Cu。
电解,,,,,,(2)Cl;H;2Cl,2e===Cl2?;2H,2e===H2?; 2H+,2C1―=====C12?,H2?。
减小;增大。
(3)Cl;Na;2Cl,2e===Cl2?;2H2O,2e===H2?,2OH;
电解,2H2O,2C1―=====C12?,H2?,2OH。增大。
(4)SO42;Cu2;2 H2O,4e===O2?,4H;Cu2++2e,Cu; ,,,,,,,,,,,
电解,2H2O,2Cu2+===== 2Cu,O2?,4H。减小。
(5)SO42;Na; 2 H2O,4e===O2?,4H; 2H2O,2e===H2?,2OH; ,,,,,,
电解2H2O===== 2H2?,O2?。不变;7。
电解,,,,,,(6)SO42;H;2H2O,4e===O2?,4H;2H,2e===H2?;2H2O===== 2H2?,O2?。
增大;增大;减小。
(7)OH;Na;4OH,4e=O2?,2H2O;2H2O,2e===H2?,2OH;
电解 2H2O===== 2H2?,O2?。增大;增大;增大。
二((1)2Cl,2e===Cl2?;氧化。2H,2e===H2?;还原。 (3)烧碱、氯气、氢气
2((1)阴、阳; (2)AgNO3溶液等含镀层金属阳离子的盐溶液
(3)Ag,e===Ag;Ag,e===Ag (4)阳、阴、不变 ——————————————————————————————————————
------------------------------------------------------------------------------------------------
3((1)粗铜 纯铜 (3)Cu,2e===Cu2;Cu2,2e===Cu ,,,,,,,,,,,,,,,,,,
4((1)2Cl,2e===Cl2?; 2Na,2e===2Na
(2)6O2,12e===3O2?; 4Al3,12e===4Al ,,,,,,,,
三. (1)Cu2++2e,Cu; 2C1――2e,C12 ;4OH,4e,2H2O+O2?; 2Ag++2e,2Ag ,,,,,
(2)2?2?4?1
四((1)Zn,2e,Zn2 ;2H,2e===H2? (2)Ag,e===Ag? ;Ag,e===Ag ,,,,,,,,
(3)Fe,2e,Fe2+; 2H,2e===H2? (4)2I―2e,I2 ;2H,2e===H2? ,,,―,,,
3
——————————————————————————————————————
范文四:原电池电极反应式电解池电极反应式电化学电极反应式书写竞赛
<涨停炒股软件>免费使用进行中,所有用户下载安装,点试用用户登录按钮就可以使用了,超强指标,超强功能,炒股利器,机会难得。网盘下载地址:http://yunpan.cn/lk/sV8ErRKmIarQu;软件官网:http://www.zbwrj.net/ztbrj/index.html
<涨停炒股软件>免费使用进行中,所有用户下载安装,点试用用户登录按钮就可以使用了,超强指标,超强功能,炒股利器,机会难得。网盘下载地址:http://yunpan.cn/lk/sV8ErRKmIarQu;软件官网:http://www.zbwrj.net/ztbrj/index.html
电化学电极反应式书写竞赛
学习小组:第( )小组 姓名:________________座号:________
(注意:该考试为闭卷考试,严禁翻书、资料或同学讨论,考生独立完成,请自律! , 班级前 10名:小组和个人加 2分, 10到 20名,加 1分;倒数 10名,小组和个人扣 1分) (每个反应式 1分,共 125分)
一、写出下列原电池电极反应式和总反应方程式 (注意离子方程式和化学方程式) 一次电池部分:(每空 1分共 27分 )
1、伏打电池:(负极 — Zn 、正极 — Cu 、电解液 — H 2SO 4) 负极: 正极: 总离子方程式 2、铁碳电池:(负极 — Fe 、正极 — C 、酸性溶液,析氢腐蚀 ) 负极: 正极:
总离子方程式: 3、铁碳电池:(负极 — Fe 、正极 — C 、电解液中性或碱性 , 吸氧腐蚀 ) 负极: 正极:
总化学方程式:
4、普通锌锰干电池:(负极 — Zn 、正极 — C 、电解液 NH 4Cl 、 MnO 2的糊状物 ) 负极: 正极:
总化学方程式:
5、碱性锌锰干电池:(负极 — Zn 、正极 — C 、电解液 KOH 、 MnO 2的糊状物) 负极: 正极:
总化学方程式: 6、银锌电池:(负极 — Zn 、正极 --Ag 2O 、电解液 NaOH) 负极: 正极:
总化学方程式:
7、铝 – 空气 – 海水 (负极 --铝、正极 --石墨、铂网等能导电的惰性材料、电解液 --海水) 负极: 正极: 总反应式为: 8、镁 ---铝电池(负极 --Al 、正极 --Mg 电解液 KOH ) 负极 (Al): 正极 (Mg) : 总化学方程式: 9、锂电池一型:(负极 --金属锂、正极 --石墨、电解液 LiAlCl 4-SOCl 2) 负极: 正极:
总化学方程式: 二次电池部分:(每空 1分共 25分 )
10、铅蓄电池:(负极 — Pb 正极 — PbO 2电解液 — 浓硫酸) 负极: 正极: 充电时阴极: 充电时阳极: 总化学方程式 ________________________
________________________
11、铁 --镍电池:(负极 --Fe 、正极 — NiO 2、电解质溶液为 KOH 溶液) 负极: 正极: 充电时阴极: 充电时阳极: 总化学方程式 ________________________
________________________
12、 LiFePO 4电池 (正极 — LiFePO 4、 FePO 4,负极 — 石墨,含 Li +导电固体为电解质) 负极: 正极: 充电时阴极: 充电时阳极: 总化学方程式 ________________________
________________________
13、镍 --镉电池 (负极 --Cd 、正极 — NiOOH 、电解质溶液为 KOH 溶液) 负极: 正极:
充电时阴极: 充电时阳极: 总化学方程式 ________________________
________________________
14、高铁电池:(负极 — Zn 、正极 ---石墨、 K 2FeO 4,电解质为浸湿固态碱性物质) 负极: 正极: 充电时阴极: 充电时阳极: 总化学方程式 ________________________________________________
燃料电池部分 (每空 1分共 33分 ) 15、氢氧燃料电池
1、电解质是 KOH 溶液 (碱性电解质)
负极: 正极: 总反应方程式:
2、电解质是 H 2SO 4溶液 (酸性电解质)
负极: 正极:
总反应方程式: 16、甲醇燃料电池
1.碱性电解质 (铂为两极、电解液 KOH 溶液) 正极: 负极: 总反应方程式 2. 酸性电解质 (铂为两极、电解液 H 2SO 4溶液) 正极: 负极: 总反应化学方程式
<涨停炒股软件>免费使用进行中,所有用户下载安装,点试用用户登录按钮就可以使用了,超强指标,超强功能,炒股利器,机会难得。网盘下载地址:http://yunpan.cn/lk/sV8ErRKmIarQu;软件官网:http://www.zbwrj.net/ztbrj/index.html
<涨停炒股软件>免费使用进行中,所有用户下载安装,点试用用户登录按钮就可以使用了,超强指标,超强功能,炒股利器,机会难得。网盘下载地址:http://yunpan.cn/lk/sV8ErRKmIarQu;软件官网:http://www.zbwrj.net/ztbrj/index.html
17、肼燃料电池 (铂为两极,负极:N 2H 4,正极:O 2, 电解液 KOH 溶液) 正极: 负极: 总反应方程式 18、甲烷燃料电池
1.碱性电解质 (铂为两极、电解液 KOH 溶液) 正极: 负极: 总反应方程式 2、酸性电解质 (铂为两极、电解液 H 2SO 4溶液) 正极: 负极:
总反应化学方程式
19、 丙烷燃料电池(铂为两极、正极通入 O 2和 CO 2、负极通入丙烷、电解液有三种) 1、电解质是熔融碳酸盐(K 2CO 3或 Na 2CO 3)
正极: - 负极:
总反应化学方程式 2、酸性电解质(电解液 H 2SO 4溶液)
正极: 负极:
总反应化学方程式 3、碱性电解质 (铂为两极、电解液 KOH 溶液) 正极: 负极:
总反应方化学程式 20、 CO 燃料电池(总反应方程式均为:2CO +O 2=2CO 2)
1、熔融盐 (铂为两极、 Li 2CO 3和 Na 2CO 3的熔融盐作电解质, CO 为负极燃气, 空气与 CO2的混合气为正极助燃气)
正极: 负极: 总反应化学方程式:
二、用惰性电极电解下列溶液,写出电解电极反应式和总反应方程式 (注意离子方程 式和化学方程式) (每空 1分共 31分 ) 1.电解 CuCl 2溶液
阳极: 阴极:
总反应离子方程式: 2.电解精炼铜(5分)
阳极(粗铜) : 、
阴极 (纯铜 ) : 3.电镀铜
阳极(纯铜) :
阴极(待镀金属,如 Fe ) : 4.电解饱和食盐水
阳极: 阴极:
总反应离子方程式:
5.电解 HCl 溶液
阳极: 阴极:
总反应离子方程式: 6.电解 NaOH 溶液
阳极: 阴极:
总反应离子方程式: 7.电解 H 2SO 4溶液
阳极: 阴极:
总反应离子方程式: 8.电解 KNO 3溶液
阳极: 阴极:
总反应离子方程式: 9.电解 CuSO 4溶液
阳极: 阴极:
总反应离子方程式: 10.电解 AgNO 3溶液
阳极: 阴极:
总反应离子方程式:
三、写出用惰性电极电解熔融状态的 Al 2O 3、 MgCl 2、 NaCl 电解电极及总反应式(每空 1分,共 9分) 11.
阳极: 阴极:
总反应化学式: 12. 2
阳极: 阴极:
总反应化学式: 13. 2O 3
阳极: 阴极:
总反应化学式:
电化学电极反应式书写竞赛答案
<涨停炒股软件>免费使用进行中,所有用户下载安装,点试用用户登录按钮就可以使用了,超强指标,超强功能,炒股利器,机会难得。网盘下载地址:http://yunpan.cn/lk/sV8ErRKmIarQu;软件官网:http://www.zbwrj.net/ztbrj/index.html
<涨停炒股软件>免费使用进行中,所有用户下载安装,点试用用户登录按钮就可以使用了,超强指标,超强功能,炒股利器,机会难得。网盘下载地址:http://yunpan.cn/lk/sV8ErRKmIarQu;软件官网:http://www.zbwrj.net/ztbrj/index.html
学习小组:第( )小组 姓名:________________座号:________
(注意:该考试为闭卷考试,严禁翻书、资料或同学讨论,考生独立完成,请自律! , 班级前 10名:小组和个人加 2分, 10到 20名,加 1分;倒数 10名,小组和个人扣 1分) (每个反应式 1分,共 128分)
一、写出下列原电池电极反应式和总反应方程式 (注意离子方程式和化学方程式) 一次电池部分:
1、伏打电池:(负极 — Zn 、正极 — Cu 、电解液 — H 2SO 4) 负极:Zn – 2e -=Zn2+ 正极:2H ++2e-=H2↑
总离子方程式 Zn+2H+=H2↑+Zn2+
2、铁碳电池:(负极 — Fe 、正极 — C 、酸性溶液,析氢腐蚀 ) 负极:Fe – 2e -=Fe2+ 正极:2H ++2e-=H2↑
总离子方程式 Fe+2H+=H2↑+Fe2+(析氢腐蚀 )
3、铁碳电池:(负极 — Fe 、正极 — C 、电解液中性或碱性 ) 负极:2Fe – 4e -=2Fe2+ 正极:O 2+2H2O+4e-=4 OH
总化学方程式 2Fe+O2+2H2O=2Fe(OH)2(吸氧腐蚀 )
4、普通锌锰干电池:(负极 — Zn 、正极 — C 、电解液 NH 4Cl 、 MnO 2的糊状物 ) 负极:Zn – 2e -=Zn2+
正极:2MnO 2+2NH4++2e-=Mn2O 3+H2O+2NH3↑
总化学方程式 Zn+2NH4Cl+2MnO2=ZnCl2+Mn2O 3+2NH3↑
5、碱性锌锰干电池:(负极 — Zn 、正极 — C 、电解液 KOH 、 MnO 2的糊状物) 负极:Zn+2OH– 2e -=Zn(OH)2
正极:2MnO 2+2H2O+2e-=2MnOOH+2OH-
总化学方程式 Zn+2MnO2+2H2O=Zn(OH)2+MnOOH 6、银锌电池:(负极 — Zn 、正极 --Ag 2O 、电解液 NaOH) 负极:Zn+2OH– – 2e -=Zn(OH)2 正极:Ag 2O+H2O+2e-=2Ag+2OH-
总化学方程式 Zn+Ag2O+H2O=Zn(OH)2+2Ag
7、铝 – 空气 – 海水 (负极 --铝、正极 --石墨、铂网等能导电的惰性材料、电解液 --海水)
负极:4Al -12e -=4Al3+
正极:3O 2+6H2O+12e-
=12OH-
总反应式为:4Al+3O2+6H2O==4Al(OH)3
8、镁 ---铝电池(负极 --Al 、正极 --Mg 电解液 KOH ) 负极 (Al):2Al+8OH– -6e -=2AlO 2– +4H2O 正极 (Mg) :6H 2O+6e-=3H 2↑+6OH–
总化学方程式:2Al+2OH– +2H2O =2AlO 2– +3H2
9、锂电池一型:(负极 --金属锂、正极 --石墨、电解液 LiAlCl 4-SOCl 2) 负极:8Li -8e -
=8Li +
正极:3SOCl 2+8e -
=SO 32-
+2S +6Cl -
总化学方程式 8Li +3SOCl 2==Li2SO 3+6LiCl +2S , 二次电池部分:
10、铅蓄电池:(负极 — Pb 正极 — PbO 2电解液 — 浓硫酸) 负极:Pb -2e -
+SO 42-
=PbSO4
正极:PbO 2+2e -
+4H +
+SO 42-
=PbSO4+2H 2O
充电时阴极:PbSO 4+2e -=Pb+ SO42-
充电时阳极:PbSO 4+2H2O -2e -=PbO2+H2SO 4+2H+ 总化学方程式 Pb +PbO 2+2H2SO 4
2PbSO 4+2H2O
11、铁 --镍电池:(负极 --Fe 、正极 — NiO 2、电解质溶液为 KOH 溶液) 负极:Fe -2e — +2OH – =Fe(OH)2 正极:NiO 2+2H2O+2e — =Ni(OH)2+2OH – 充电时阴极:Fe(OH)2+2e — =Fe+2OH –
充电时阳极:Ni(OH)2-2e — +2OH – =NiO2+2H2O 总化学方程式 Fe+NiO2+2H2O
Fe(OH)2+Ni(OH)2
12、 LiFePO 4电池 (正极 — LiFePO 4 、 FePO 4,负极 — 石墨,含 Li +导电固体为电解质) 放电时负极:Li -e — =Li+ 正极:FePO 4+Li++e— =LiFePO4 充电时阴极:Li ++e— =Li
充电时阳极:LiFePO 4-e — =FePO4+Li+ 总化学方程式 FePO 4+Li
LiFePO 4
13、镍 --镉电池 (负极 --Cd 、正极 — NiOOH 、电解质溶液为 KOH 溶液)
放电时负极:Cd -2e — +2OH – =Cd(OH)2
正极:2NiOOH+2e — +2H2O=2Ni(OH)2+2OH– 充电时阴极:Cd(OH)2+2e — =Cd+2OH –
充电时阳极:2Ni(OH)2-2e — +2OH – =2NiOOH+2H2O 总化学方程式 Cd+2NiOOH+2H2O
Cd(OH)2+2Ni(OH)2
14、高铁电池:(负极 — Zn 、正极 ---石墨、 K 2FeO 4, 电解质为浸湿固态碱性物质) 放电时负极:3Zn -6e -+6OH– =3Zn(OH)2 正极:2FeO 42— +6e -+8H2O=2Fe(OH)3+10OH– 充电时阴极:3Zn(OH)2+6e -=3Zn+6OH–
充电时阳极:2Fe(OH)3-6e -+10OH– =2FeO42— +8H2O 总化学方程式 3Zn+2K2FeO 4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH
燃料电池部分 15、氢氧燃料电池
1、电解质是 KOH 溶液 (碱性电解质) 负极:H 2– 2e -+2OH— ==2H2O 正极:O 2+2H2O+4e-==4OH— 总反应方程式 2H 2+O2==2H2O 2、电解质是 H 2SO 4溶液 (酸性电解质) 负极:H 2– 2e -==2H+ 正极:O 2+4H++4e-==2H2O
总反应方程式 2H 2+O2==2H2O 16、甲醇燃料电池
1.碱性电解质 (铂为两极、电解液 KOH 溶液) 正极:3O 2+12e-+6H20==12OH-
负极:2CH 3OH – 12e -+16OH— ==2CO32-+12H2O 总反应方程式 2CH 3OH+3O2+4KOH==2K2CO 3+6H2O 2. 酸性电解质 (铂为两极、电解液 H 2SO 4溶液)
正极:3O 2+12e-+12H+=6H2O (注:乙醇燃料电池与甲醇燃料电池原理基本相) 负极:2CH 3OH – 12e -+2H2O=12H++2CO2
总反应化学方程式 2CH 3OH+3O2==2CO2+4H2O
17、肼燃料电池 (铂为两极、负极:N 2H 4正极:O 2, 电解液 KOH 溶液)
<涨停炒股软件>免费使用进行中,所有用户下载安装,点试用用户登录按钮就可以使用了,超强指标,超强功能,炒股利器,机会难得。网盘下载地址:http://yunpan.cn/lk/sV8ErRKmIarQu;软件官网:http://www.zbwrj.net/ztbrj/index.html
<涨停炒股软件>免费使用进行中,所有用户下载安装,点试用用户登录按钮就可以使用了,超强指标,超强功能,炒股利器,机会难得。网盘下载地址:http://yunpan.cn/lk/sV8ErRKmIarQu;软件官网:http://www.zbwrj.net/ztbrj/index.html
正极:O 2+2H2O+4e-=4OH— 负极:N 2H 4+4OH— --4e -=N2+4H2O 总反应方程式 N 2H 4+O2==N2+2H2O 18、甲烷燃料电池
1.碱性电解质 (铂为两极、电解液 KOH 溶液) 正极:2O 2+2H2O+8e-=8OH— 负极:CH 4+10OH— --8e -=CO32-+7H2O
总反应方程式 CH 4+2KOH+2O2==K2CO 3+3H2O 2、酸性电解质 (铂为两极、电解液 H 2SO 4溶液) 正极:2O 2+8e-+8H+=4H2O 负极:CH 4--8e -+2H2O=8H++CO2 总反应化学方程式 CH 4+2O2==CO2+2H2O
19、 丙烷燃料电池(铂为两极、正极通入 O 2和 CO 2、负极通入丙烷、电解液有三种) 1、电解质是熔融碳酸盐(K 2CO 3或 Na 2CO 3) 正极:5O 2+20e-+10CO2=10CO32- 负极:C 3H 8-20e -+10CO32-=3CO2+4H2O 总反应化学方程式 C 3H 8+5O2==3CO2+4H2O 2、酸性电解质(电解液 H 2SO 4溶液) 正极:5O 2+20e-+20H+=10H2O 负极:C 3H 8-20e -+6H2O=3CO2+20H+ 总反应化学方程式 C 3H 8+5O2==3CO2+4H2O 3、碱性电解质 (铂为两极、电解液 KOH 溶液) 正极:5O 2+20e-+10H2O=20OH— 负极:C 3H 8--20e -+26OH— =3CO32-+17H2O
总反应方化学程式 C 3H 8+5O2+6KOH==3K2CO 3+7H2O 20、 CO 燃料电池(总反应方程式均为:2CO +O 2=2CO 2)
1、熔融盐 (铂为两极、 Li 2CO 3和 Na 2CO 3的熔融盐作电解质, CO 为负极燃气, 空气与 CO2的混合气为正极助燃气) 正极:O 2+4e -+2CO 2=2CO 32-- 负极:2CO +2CO 32-– 4e -=4CO2
总反应化学方程式:2CO +O 2=2CO 2
二、用惰性电极电解下列溶液,写出电解电极反应式和总反应方程式 (注意离子方程 式和化学方程式) 1.电解 CuCl 2溶液 阳极:2Cl --2e -
=Cl2↑ 阴极:Cu 2++2e-=Cu
总反应离子方程式:2Cl -+Cu2+Cl 2↑+Cu
2.电解精炼铜
阳极(粗铜) :Cu-2e -=Cu2+ Fe-2e -
=Fe2+
Zn-2e -=Zn2+ Ni-2e -
=Ni2+
阴极 (纯铜 ) :Cu 2++2e-=Cu
3.电镀铜
阳极(纯铜) :Cu-2e -
=Cu2+
阴极(待镀金属,如 Fe ) :Cu 2++2e-
=Cu 4.电解饱和食盐水 阳极:2Cl --2e -
=Cl2↑ 阴极:2H ++2e-=H2↑
总反应离子方程式:2Cl -
+2H2O H 2↑+Cl2↑+2OH
-
5.电解 HCl 溶液 阳极:2Cl --2e -
=Cl2↑ 阴极:2H ++2e-=H2↑
总反应离子方程式:2Cl -
+2H+
Cl 2↑+H2↑
6.电解 NaOH 溶液 阳极:4OH --4e -
=O2↑+2H2O 阴极:4H ++4e-=2H2↑
总反应离子方程式:2H 2O 2H 2↑+O2↑
7.电解 H 2SO 4溶液 阳极:4OH --4e -
=O2↑+2H2O 阴极:4H ++4e-=2H2↑
总反应离子方程式:2H 2O 2H 2↑+O2↑
8.电解 KNO 3溶液 阳极:4OH --4e -
=O2↑+2H2O
阴极:4H ++4e-
=2H2↑
总反应离子方程式:2H 2O 2H 2↑+O2↑
9.电解 CuSO 4溶液 阳极:4OH --4e -
=O2↑+2H2O 阴极:2Cu 2++4e-=2Cu
总反应式:2Cu 2++2H2O 2Cu+O2↑+4H+
10.电解 AgNO 3溶液
阳极:4OH --4e -
=O2↑+2H2O 阴极:4Ag ++4e-
=4Ag
总反应离子方程式:4Ag ++2H2O 4Ag+O2↑+4H+
三、写出用惰性电极电解熔融状态的 Al 2O 3、 MgCl 2、 NaCl 电解电极及总反应式 11.
阳极:2Cl --2e -=Cl2↑ 阴极:2Na ++2e-=2Na 总反应化学式:2NaCl(熔融 ) 2Na+Cl2↑
12. 2
阳极:2Cl --2e -=Cl2↑ 阴极:Mg 2++2e-=Mg 总反应化学式:MgCl 2(熔融 ) Mg+Cl 2↑
13. 2O 3
阳极:6O 2--12e -=3O2↑ 阴极:4Al 3++12e-=4Al 总反应化学式:2Al 2O 3(熔融 ) 4Al+3O2↑
范文五:电镀铜的电极反应式(共4篇)
以下是网友分享的关于电镀铜的电极反应式的资料4篇,希望对您有所帮助,就爱阅读感谢您的支持。
电池电极反应式或总反应式的书写篇1
电池电极反应式或总反应式的书写
1.铝—镍电池(负极—Al,正极—Ni,电解液—NaCl溶液、O2) 负极:4Al,12e===4Al;
正极:3O2,6H2O,12e===12OH;
总反应式:4Al,3O2,6H2O===4Al(OH)3。
2.镁—铝电池(负极—Al,正极—Mg,电解液—KOH溶液)
负极:2Al,8OH,6e===2AlO,4H2O;
正极:6H2O,6e===3H2?,6OH;
总反应离子方程式:2Al,2OH,2H2O===2AlO,3H2?。
1
3.锂电池一型(负极—Li,正极—石墨,电解液—LiAlCl4—SOCl2) 已知电池总反应式:4Li,2SOCl2===SO2?,4LiCl,S。试写出正、负极反应式: 负极:4Li,4e===4Li;
正极:2SOCl2,4e===SO2?,S,4Cl。
4.铁—镍电池(负极—Fe,正极—NiO2,电解液—KOH溶液)
放电已知Fe,NiO2,2H2O 充电Fe(OH)2,Ni(OH)2,则:
负极:Fe,2e,2OH===Fe(OH)2;
正极:NiO2,2H2O,2e===Ni(OH)2,2OH。
阴极:Fe(OH)2,2e===Fe,2OH;
阳极:Ni(OH)2,2e,2OH===NiO2,2H2O。
5.LiFePO4电池(正极—LiFePO4,负极—Li,含Li导电固体为电解质)
放电已知FePO4,Li 充电LiFePO4,则
负极:Li,e===Li;
正极:FePO4,Li,e===LiFePO4。
阴极:Li,e===Li;
阳极:LiFePO4,e===FePO4,Li。
6.高铁电池(负极—Zn,正极—石墨,电解质为浸湿的固态碱性物质)
2
放电已知:3Zn,2K2FeO4,8H2O 充电3Zn(OH)2,2Fe(OH)3,4KOH,则:
负极:3Zn,6e,6OH===3Zn(OH)2;
正极:2FeO,6e,8H2O===2Fe(OH)3,10OH。
阴极:3Zn(OH)2,6e===3Zn,6OH;
阳极:2Fe(OH)3,6e,10OH===2FeO8H2O。
7.氢氧燃料电池
(1)电解质是KOH溶液(碱性电解质)
负极:2H2,4e,4OH===4H2O;
1
,,,,2,,,2,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,,3,
正极:O2,2H2O,4e===4OH;
总反应方程式:2H2,O2===2H2O。
(2)电解质是H2SO4溶液(酸性电解质)
负极:2H2,4e===4H;
正极:O2,4H,4e===2H2O;
总反应方程式:2H2,O2===2H2O。
(3)电解质是NaCl溶液(中性电解质)
负极:2H2,4e===4H;
正极:O2,2H2O,4e===4OH;
总反应方程式:2H2,O2===2H2O。
3
8.甲烷燃料电池(铂为两极、正极通入O2和CO2、负极通入甲烷、电解液有三种)
(1)电解质是熔融碳酸盐(K2CO3或Na2CO3)
正极:2O2,8e,4CO2===4CO3;
负极:
总反应方程式:CH4,2O2===CO2?,2H2O。
(2)酸性电解质(电解液为H2SO4溶液)
正极:2O2,8e,8H===4H2O;
负极:CH4,8e,2H2O===CO2?,8H;
总反应方程式:CH4,2O2===CO2?,2H2O。
(3)碱性电解质(铂为两极、电解液为KOH溶液)
正极:2O2,8e,4H2O===8OH;
负极:CH4,8e,10OH===CO7H2O;
总反应方程式:CH4,2O2,2OH===CO3,3H2O。
9.甲醇燃料电池
(1)碱性电解质(铂为两极、电解液为KOH溶液)
正极:3O2,12e,6H2O===12OH;
总反应方程式:2CH3OH,3O2,4KOH===2K2CO3,6H2O。
(2)酸性电解质(铂为两极、电解液为H2SO4溶液)
正极:3O2,12e,12H===6H2O;
负极:2CH3OH,12e,2H2O===12H,2CO2;
4
总反应方程式:2CH3OH,3O2===2CO2,4H2O。
10.CO燃料电池(总反应方程式均为2CO,O2===2CO2)
(1)熔融盐(铂为两极、Li2CO3和Na2CO3的熔融盐作电解质,CO为负极燃气,空气与CO2的
2
,,,,,,2,,,,2,,,2,,,,,,,,2,,2,,,,,,,,,,,
混合气为正极助燃气)
正极: 负极:(2)酸性电解质(铂为两极、电解液为H2SO4溶液) 正极:O2,4e,4H===2H2O; 负极:2CO,4e,2H2O===2CO2,4H。
电解池电极反应式的书写
1.用惰性电极电解下列溶液
(1)NaCl溶液
阴极:2H,2e===H2?;
阳极:2Cl,2e===Cl2?;
电解总反应式:2NaCl,2H22NaOH,H2?,Cl2?。
(2)CuSO4溶液
阴极:2Cu,4e===2Cu; 阳极:4OH,4e===2H2O,O2?;
电解总反应式:2CuSO4,2H22Cu,2H2SO4,O2?。
2.用惰性电极电解下列熔融态物质
5
(1)MgCl2
阳极:2Cl,2e===Cl2?; 阴极:Mg,2e===Mg;
电解总反应式:MgCl2(熔融)=====Mg,Cl2?。
(2)Al2O3
阳极:6O,12e===3O2?; 阴极:4Al,12e===4Al;
电解总反应式:2Al2O3(熔融)=====4Al,3O2?。
3.用铜作电极电解下列溶液
(1)H2O
阴极:2H,2e===H2?;
阳极:Cu,2e===Cu;
电解总反应式:Cu,2H2O=====Cu(OH)2?,H2?。
(2)H2SO4溶液
阴极:2H,2e===H2?;
阳极:Cu,2e===Cu;
3
,2,,,,2,,,3,,2,,2,,,,,,2,,,,,,,,,,2,,,2,
电解总反应式:Cu,H2SO4=====CuSO4,H2?。
(3)NaOH溶液
阴极:2H2O,2e===H2?,2OH; 阳极:Cu,2e,2OH===Cu(OH)2?;
电解总反应式:Cu,2H2O=====Cu(OH)2?,H2?。
6
4.用Al作电极电解下列溶液
(1)H2SO4溶液
阴极:6H,6e===3H2?; 阳极:2Al,6e===2Al;
电解总反应式:2Al,3H2SO4=====Al2(SO4)3,3H2?。
(2)NaOH溶液
阴极:6H2O,6e===3H2?,6OH; 阳极:2Al,6e,8OH===2AlO,4H2O;
电解总反应式:2Al,2H2O,2NaOH=====2NaAlO2,3H2?。
,,,,,,3,,,,,,,
4
电极反应式和总反应式的书写规范篇2
电极反应式和总反应式的书写规范
关于高中化学的电化学部分一直是高中化学内容中重要的基本概念和基础理论之一,特别是电极反应式和总反应式的书写问题。虽说现行新课程对这部分的要求不高,但是,这部分的内容一直是高考和竞赛的要点和难点。再加上现行教材中对这部分的内容书写也不是很规范,这样更加加大了教师和学生教与学的难度。本文旨在唤起广大师生的共识,力
7
求规范和准确书写电极反应式和总反应式。
一、电极反应式和总反应式的一般概念
电极反应式是指在电化学反应中,原电池放电时的正、负极(或电解池电解时的阴、阳极)发生的还原、氧化反应得失电子的离子反应式(包括极区溶液中的微粒参加的反应在内)。其实质均是将氧化还原反应分割成氧化和还原两个半反应的反应式,并且伴随着电子的得失和转移。
总反应式则有两个层次的含义。广义的总反应式是指原电池放电(或电解池电解)时装置中所发生的所有相关化学变化并反映各物质之间的化学计量关系的总反应式(既包括两极反应又包括两极反应的产物在溶液中的相关反应)。而狭义的总反应式仅是指两电极反应式之和,不包括两极的电极反应产物在溶液中相遇或混匀溶液时发生的反应。
例如:普通的锌锰干电池的电极反应式和总反应式如下:
正极:2NH4+ + 2e- + 2MnO2 = 2NH3 + Mn2O3 + H2O
(包括极区反应H2+2MnO2=Mn2O3+H2O,教材此处已在试用版的基础上得到修正)
负极:Zn - 2e- = Zn2+
该电池总反应式为(狭义):Zn + 2NH4+ + 2MnO2 = Zn2+
+ 2NH3 + Mn2O3 + H2O(一般常用此式表示)
若还包括两极各自产物Zn2+和NH3在溶液中的络合反应
8
{ Zn2+ + 4NH3 =
[Zn(NH3)4]2+},则该电池反应的总反应式(广义)即为:2Zn + 4NH4+ + 4MnO2 = Zn2+ +[Zn(NH3)4]2+ + 2Mn2O3 +2 H2O。
二、电极反应式和总反应式的书写规则
1、电极反应式的书写规则
(1)原电池放电时的正、负极(或电解池电解时的阴、阳极)的电极反应式中各微粒的化学式均严格按照离子方程式的书写规则进行书写(即除了易溶且易电离的物质才可拆成离子形式,其它物质一律只写成化学式)。
(2)电极反应式不仅写出被氧化和被还原的物质及其产物外,还须包括该极区周围电解质溶液中参加了离子反应的微粒在内。(注意:由于盐类的水解程度一般很小,因此可不考虑某些离子的水解反应)
(3)原电池放电时的正、负极(或电解池电解时的阴、阳极)的电极反应式都应满足氧化还原反应的电子得失守衡。
例1:氢氧燃料电池
(1)在KOH溶液的强碱性介质中
负极: 2H2 - 4e - + 4OH - = 4H2O
? ?
(被氧化物质) (负极区溶液中的OH - 和氧化产物H+反应)
9
正极: O2 + 4e - + 2H2O = 4OH -
? ?
(被还原物质) (正极区溶液中的H2O和还原产物反应)
(2)在盐酸的强酸性介质中
负极: 2H2 - 4e - = 4H+
正极: O2 + 4e - + 4H+ = 2H2O
? ?
(被还原物质) (正极区溶液中的H+和还原产物反应) 例2:用惰性电极电解
(1)Na2SO4溶液:
阳极:2H2O - 4e - = 4H+ + O2? (导致阳极区周围溶液呈酸性)
阴极:4H2O + 4e - = 2H2? + 4OH - (导致阴极区周围溶液呈碱性)
(当溶液中阳极产物H+和阴极产物OH-在溶液中相遇发生反应H+ + OH- = H2O,最终溶液呈中性)
(2)H2SO4溶液:
阳极:2H2O - 4e - = 4H+ + O2?
阴极:4H+ + 4e - = 2H2?
2、总反应式的书写规则
(1)将原电池放电时的正、负两极(或电解时的阴、阳两
10
极)的电极反应式相加所得的和即为总反应式(这里系指狭义的总反应式)。
(2)电解质溶液中来自两极的电极反应所分别产生的离子,在溶液中相向迁移,相遇并相互发生的离子反应,可单独书写离子方程式,当然也可写入总反应式而得到广义的总反应式(由于这些离子反应的化学计量数关系和电极反应式是一致的)。
上述例1的电池总反应式均为:2H2 + O2 = 2H2O; 而例2的广义总反应式均为:2H2
O 2H2? + O2?
(3)以上所得的总反应式一般为离子方程式,也可改写成对应的化学方程式。
三、教材中相关内容的规范书写
1.铅蓄电池:
(1)放电时:
负极:Pb - 2e- + SO42- = PbSO4
? ?
(被氧化物质) (负极区溶液中的SO42-和氧化产物Pb2+反应)
正极:PbO2 + 2e- + 4H+ + SO42- = PbSO4 + 2H2O
? ? ?
(被还原物质) (正极区溶液中的H+、SO42-和还原产
11
物反应)
(2)充电时:
阳极:PbSO4 + 2H2O - 2e- = PbO2 + 4H+ + SO42-
阴极:PbSO4 + 2e- = Pb + SO42-
总反应式为:Pb + PbO2 + 2H2SO4
2.电解饱和食盐水:
阳极:2Cl- - 2e- = Cl2?
阴极:2H2O + 2e- = H2? + 2OH-(导致阴极区周围溶液呈碱性。此处教材里书写不规范)
总离子反应式:2Cl- + 2H2
O
总化学方程式为:2NaCl + 2H2
O
四、下列实例,以作规范参考和对照比较
例1:将用导线相连的表面已经过活化的铂电极插入KOH溶液中,然后向两极分别通入CH3OH和O2,构成甲醇燃料电池。该电池的电极反应式和总反应式分别为:
负极:2CH3OH - 12e- + 16OH- = 2CO32- + 12H2O
正极:3O2 + 12e- + 6H2O = 12OH-
电池总反应式为:2CH3OH + 3O2 + 4OH- = 2CO32- +
6H2O
12
例2:用电化学方法制备KIO3的原理是:以石墨电极为阳极,不锈钢电极Cl2? + H2?+ 2OH- Cl2? + H2?+ 2NaOH 2PbSO4 + 2H2O
为阴极,用KI溶液(加入少量K2Cr2O7)为电解质溶液,在一定电流强度和温度下进行电解,其电解总反应式为:
KI + 3H2O KIO3+3H2?。其两极反应式为:
阴极:6H2O + 6e- = 3H2? + 6OH-
阳极:I- + 3H2O - 6e- = IO3- + 6H+
例3:银器皿日久表面逐渐变为黑色,这是由于生成了Ag2S,有人设计用原电池原理除去银器表面黑色,让其重放光彩。其处理方法是:将一定浓度的食盐溶液放入一铝制容器中,再将变黑的银器浸入溶液中,放置一段时间后,黑色会逐渐褪去而银却不会损失。该原电池中:
负极:2Al - 6e- = 2Al3+
正极:3Ag2S + 6e- = 6Ag + 3S2-
该电池总反应式(广义)为:2Al + 3Ag2S + 6H2O = 2Al(OH)3 ?+ 3H2S?+ 6Ag(包括正、负极产物Al3+和S2-在溶液中的双水解反应:2Al3+ + 3S2- + 6H2O = 2Al(OH)3
?+ 3H2S?在内)
五、电极反应式和总反应式的书写规范的必要性
作为一门基础科学的教材,首先要注重规范。虽然教材在原有的基础上也在逐渐修正,但还须及时和加强。其次,教
13
师在教学过程中更要力求化学用语的规范化书写,要讲清概念、定义、原理的内涵和外延,并加强巩固和训练,提高学生书面语言的准确性、规范性,让学生养成认真严谨的科学态度,减少学生因文字和化学用语表达不具体、不规范等非智力因素而造成不必要的失误
电极反应式和总反应式的书写规范篇3
电极反应式和总反应式的书写规范
作者:hxfdz 文章来源:本站原创 点击数:130 更新时间:2008-8-16
关于高中化学的电化学部分一直是高中化学内容中重要的基本概念和基础理论之一,特别是电极反应式和总反应式的书写问题。虽说现行新课程对这部分的要求不高,但是,这部分的内容一直是高考和竞赛的要点和难点。再加上现行教材中对这部分的内容书写也不是很规范,这样更加加大了教师和学生教与学的难度。本文旨在唤起广大师生的共识,力求规范和准确书写电极反应式和总反应式。
一、电极反应式和总反应式的一般概念
电极反应式是指在电化学反应中,原电池放电时的正、负极(或电解池电解时的阴、阳极)发生的还原、氧化反应得失电子的离子反应式(包括极区溶液中的微粒参加的反应在
14
内)。其实质均是将氧化还原反应分割成氧化和还原两个半反应的反应式,并且伴随着电子的得失和转移。
总反应式则有两个层次的含义。广义的总反应式是指原电池放电(或电解池电解)时装置中所发生的(((
所有相关化学变化并反映各物质之间的化学计量关系的总反应式(既包括两极反应又包括两极反应的产物在溶液中的相关反应)。而狭义的总反应式仅是指两电极反应式之和,不包括两极的电极反应产物在溶液中(((
相遇或混匀溶液时发生的反应。
例如:普通的锌锰干电池的电极反应式和总反应式如下:
正极:2NH4+ + 2e- + 2MnO2 = 2NH3 + Mn2O3 + H2O
(包括极区反应H2+2MnO2=Mn2O3+H2O,教材此处已在试用版的基础上得到修正)
负极:Zn - 2e- = Zn2+
该电池总反应式为(狭义):Zn + 2NH4+ + 2MnO2 = Zn2+
+ 2NH3 + Mn2O3 + H2O(一般常用 此式表示)
若还包括两极各自产物Zn2+和NH3在溶液中的络合反应{ Zn2+ + 4NH3 = [Zn(NH3)4]2+},则该电池反应的总反应式(广义)即为:2Zn + 4NH4+ + 4MnO2 = Zn2+ +[Zn
(NH3)4]2+ + 2Mn2O3 +2 H2O。
二、电极反应式和总反应式的书写规则
1、电极反应式的书写规则
15
(1)原电池放电时的正、负极(或电解池电解时的阴、阳极)的电极反应式中各微粒的化学式均严格按照离子方程式的书写规则进行书写(即除了易溶且易电离的物质才可拆成离子形式,其它物质一律只写成化学式)。
(2)电极反应式不仅写出被氧化和被还原的物质及其产物外,还须包括该极区周围电解质溶液中参加了离子反应的微粒在内。(注意:由于盐类的水解程度一般很小,因此可不考虑某些离子的水解反应)
(3)原电池放电时的正、负极(或电解池电解时的阴、阳极)的电极反应式都应满足氧化还原反应的电子得失守衡。
例1:氢氧燃料电池
(1)在KOH溶液的强碱性介质中
负极: 2H2 - 4e - + 4OH - = 4H2O
? ?
(被氧化物质) (负极区溶液中的OH - 和氧化产物H+反应)
正极: O2 + 4e - + 2H2O = 4OH -
? ?
(被还原物质) (正极区溶液中的H2O和还原产物反应)
(2)在盐酸的强酸性介质中
负极: 2H2 - 4e - = 4H+
正极: O2 + 4e - + 4H+ = 2H2O
16
? ?
(被还原物质) (正极区溶液中的H+和还原产物反应)
例2:用惰性电极电解
(1)Na2SO4溶液:
阳极:2H2O - 4e - = 4H+ + O2? (导致阳极区周围溶液呈酸性)
阴极:4H2O + 4e - = 2H2? + 4OH - (导致阴极区周围溶液呈碱性)
(当溶液中阳极产物H+和阴极产物OH-在溶液中相遇发生反应H+ + OH- = H2O,最终溶液呈中性)
(2)H2SO4溶液:
阳极:2H2O - 4e - = 4H+ + O2?
阴极:4H+ + 4e - = 2H2?
2、总反应式的书写规则
(1)将原电池放电时的正、负两极(或电解时的阴、阳两极)的电极反应式相加所得的和即为总反应式(这里系指狭义的总反应式)。
(2)电解质溶液中来自两极的电极反应所分别产生的离子,在溶液中相向迁移,相遇并相互发生的离子反应,可单独书写离子方程式,当然也可写入总反应式而得到广义的总反应式(由于这些离子反应的化学计量数关系和电极反应式是一
17
致的)。
上述例1的电池总反应式均为:2H2 + O2 = 2H2O;
而例2的广义总反应式均为:2H2
O 2H2? + O2?
(3)以上所得的总反应式一般为离子方程式,也可改写成对应的化学方程式。
三、教材中相关内容的规范书写
1.铅蓄电池:
(1)放电时:
负极:Pb - 2e- + SO42- = PbSO4
? ?
(被氧化物质) (负极区溶液中的SO42-和氧化产物Pb2+反应)
正极:PbO2 + 2e- + 4H+ + SO42- = PbSO4 + 2H2O
? ? ?
(被还原物质) (正极区溶液中的H+、SO42-和还原产物反应)
(2)充电时:
阳极:PbSO4 + 2H2O - 2e- = PbO2 + 4H+ + SO42-
阴极:PbSO4 + 2e- = Pb + SO42-
总反应式为:Pb + PbO2 + 2H2SO4
18
2.电解饱和食盐水:
阳极:2Cl- - 2e- = Cl2? 2PbSO4 + 2H2O
阴极:2H2O + 2e- = H2? + 2OH-(导致阴极区周围溶液呈碱性。此处教材里书写不规范) 总离子反应式:2Cl- + 2H2
O
总化学方程式为:2NaCl + 2H2
O
四、下列实例,以作规范参考和对照比较
例1:将用导线相连的表面已经过活化的铂电极插入KOH溶液中,然后向两极分别通入CH3OH和O2,构成甲醇燃料电池。该电池的电极反应式和总反应式分别为:
负极:2CH3OH - 12e- + 16OH- = 2CO32- + 12H2O
正极:3O2 + 12e- + 6H2O = 12OH-
电池总反应式为:2CH3OH + 3O2 + 4OH- = 2CO32- +
6H2O
例2:用电化学方法制备KIO3的原理是:以石墨电极为阳极,不锈钢电极为阴极,用KI溶液(加入少量K2Cr2O7)为电解质溶液,在一定电流强度和温度下进行电解,其电解总反应式为:
KI + 3H2O KIO3+3H2?。其两极反应式为:
阴极:6H2O + 6e- = 3H2? + 6OH-
阳极:I- + 3H2O - 6e- = IO3- + 6H+
19
例3:银器皿日久表面逐渐变为黑色,这是由于生成了Ag2S,有人设计用原电池原理除去银器表面黑色,让其重放光彩。其处理方法是:将一定浓度的食盐溶液放入一铝制容器中,再将变黑的银器浸入溶液中,放置一段时间后,黑色会逐渐褪去而银却不会损失。该原电池中:
负极:2Al - 6e- = 2Al3+
正极:3Ag2S + 6e- = 6Ag + 3S2-
该电池总反应式(广义)为:2Al + 3Ag2S + 6H2O =
2Al(OH)3 ?+ 3H2S?+ 6Ag(包括正、负极产物Al3+和S2-在溶液中的双水解反应:2Al3+ + 3S2- + 6H2O = 2Al(OH)3
?+ 3H2S?在内) Cl2? + H2?+ 2OH- Cl2? + H2?+ 2NaOH
五、电极反应式和总反应式的书写规范的必要性
作为一门基础科学的教材,首先要注重规范。虽然教材在原有的基础上也在逐渐修正,但还须及时和加强。其次,教师在教学过程中更要力求化学用语的规范化书写,要讲清概念、定义、原理的内涵和外延,并加强巩固和训练,提高学生书面语言的准确性、规范性,让学生养成认真严谨的科学态度,减少学生因文字和化学用语表达不具体、不规范等非智力因素而造成不必要的失误
电池电极反应式或总反应式的书写篇4
20
电池电极反应式或总反应式的书写
1(铝—镍电池(负极—Al,正极—Ni,电解液—NaCl溶液、
O2) 负极:
____________________________________________ 正极:
____________________________________________ 总反应
式:____________________________________________
2(镁—铝电池(负极—Al,正极—Mg,电解液—KOH溶
液) 负极:
____________________________________________ 正极:
____________________________________________ 总反应
离子方程式:_____________________________________
3(锂电池(负极—Li,正极—石墨,电解液
—LiAlCl4—SOCl2) 已知电池总反应式:4Li,
2SOCl2===SO2?,4LiCl,S,则 负极:
____________________________________________ 正极:
____________________________________________
4(铁—镍电池(负极—Fe,正极—NiO2,电解液—KOH
溶液) 已知Fe,NiO2,2H2O Fe(OH)2,Ni(OH)2,
则: 充电
负极:____________________________________________ 正极:____________________________________________ 阴极:____________________________________________
21
阳极:____________________________________________
5(LiFePO4电池(正极—LiFePO4,负极—Li,含Li导电
固体为电解质) 已知FePO4,Li LiFePO4,则 充电
负极:___________________________________________ 正极:____________________________________________ 阴极:____________________________________________ 阳极:____________________________________________
6(高铁电池(负极—Zn,正极—石墨,电解质为浸湿的固
态碱性物质) 已知:3Zn,2K2FeO4,
8H2O 3Zn(OH)2,2Fe(OH)3,4KOH,则: 充电
负极:____________________________________________ 正极:___________________________________________ 阴
极:____________________________________________ 阳
极:___________________________________________
7(氢氧燃料电池 放电放电,放电
(1)电解质是KOH溶液(碱性电解质)
负极:____________________________________________ 正极:__________________________________________
总反应式:
____________________________________________
(2)电解质是H2SO4溶液(酸性电解质)
负极:____________________________________________
22
正极:____________________________________________ 总反应式:
___________________________________________
(3)电解质是NaCl溶液(中性电解质)
负极:___________________________________________ 正极:____________________________________________ 总反应式:
____________________________________________
8(甲醇燃料电池
(1)碱性电解质(铂为两极、电解液为KOH溶液)
正极:____________________________________________ 负极:____________________________________________ 总反应式:
____________________________________________
(2)酸性电解质(铂为两极、电解液为H2SO4溶液)
正极:____________________________________________ 负极:___________________________________________ 总
反应式:___________________________________________
9(CO燃料电池(总反应方程式均为2CO,O2===2CO2)
(1)熔融盐(铂为两极、Li2CO3和Na2CO3的熔融盐作电解
质,CO为负极燃气,空气与CO2的混合气为正极助燃气)
正极:____________________________________________
23
负极:____________________________________________
(2)酸性电解质(铂为两极、电解液为H2SO4溶液)
正极:___________________________________________ 负极:____________________________________________
电解池电极反应式的书写
1(用惰性电极电解下列溶液
(1)NaCl溶液
阴极:___________________________________________ 阳极:____________________________________________
总反应式:
___________________________________________
(2)CuSO4溶液
阴极:____________________________________________ 阳极:___________________________________________
总反应式:
____________________________________________
2(用惰性电极电解下列熔融态物质
(1)MgCl2
阳极:____________________________________________ 阴极:___________________________________________
总反应式:
____________________________________________
24
(2)Al2O3
阳极:____________________________________________ 阴极:____________________________________________ 总反应式:
____________________________________________
3(用铜作电极电解下列溶液
(1)H2O
阴极:___________________________________________ 阳极:____________________________________________ 总反应式:
____________________________________________
(2)H2SO4溶液
阴极:____________________________________________ 阳极:____________________________________________
总反应式:
____________________________________________。
(3)NaOH溶液
阴极:____________________________________________ 阳极:___________________________________________ 总
反应式:___________________________________________
4(用Al作电极电解下列溶液
(1)H2SO4溶液
25
阴极:___________________________________________ 阳极:____________________________________________ 总反应式:
___________________________________________
(2)NaOH溶液
阴极:____________________________________________
阳极:____________________________________________ 总反应式:
___________________________________________
26



 风丶落日耀
风丶落日耀

